题目内容
16.下列各组物质的溶液,不用其他试剂,仅通过观察和用组内溶液相互混合的方法,不能将它们一一鉴别出来的是( )| A. | Ba(OH)2、NaCl、Na2SO4、Na2CO3 | B. | NaCl、BaCl2、CuSO4、NaOH | ||
| C. | NaOH、Ca(OH)2、H2SO4、K2CO3 | D. | KNO3、HCl、Na2CO3、BaCl2 |
分析 在不另加试剂就能鉴别的题目中,首先观察有无有特殊颜色的物质,若有,将有颜色的溶液鉴别出来,然后再借用这种溶液鉴别其它溶液;若都没有颜色就将溶液两两混合,根据混合后的现象进行分析鉴别.
解答 解:A、组内四种物质的溶液两两混合时,Ba(OH)2溶液与Na2SO4、Na2CO3溶液反应均能产生白色沉淀,但其余两两混合均没有明显现象,故不加其他试剂无法鉴别.
B、CuSO4溶液是蓝色的,首先鉴别出蓝色的CuSO4溶液;能与CuSO4溶液反应产生蓝色沉淀的是NaOH溶液,能与CuSO4溶液反应产生白色沉淀的是BaCl2溶液,无明显变化的是氯化钠溶液,故不加其他试剂可以鉴别.
C、组内四种物质的溶液两两混合时,其中有一种溶液与其它三种溶液混合时出现一次白色沉淀和一次放出气体,该溶液为K2CO3溶液;与K2CO3溶液产生气体的溶液为H2SO4,产生白色沉淀的为Ca(OH)2;与碳酸钠溶液混合无任何明显现象的为NaOH溶液;故不加其他试剂可以鉴别.
D、组内四种物质的溶液两两混合时,其中有一种溶液与其它三种溶液混合时出现一次白色沉淀和一次放出气体,该溶液为Na2CO3溶液;与Na2CO3溶液产生气体的溶液为HCl,产生白色沉淀的为BaCl2;与碳酸钠溶液混合无任何明显现象的为KNO3溶液;故不加其他试剂可以鉴别.
故选:A.
点评 解答不另加试剂就能鉴别的题目时,若选项中有带色的离子,首先鉴别,然后再鉴别其它的物质;若都没有颜色,可将溶液两两混合,根据混合后的现象进行鉴别.

练习册系列答案
相关题目
7.下列分类正确的是( )
| A. | 橡胶、塑料、纤维都是合成材料 | |
| B. | 硝酸钾、尿素、磷酸铵都是复合肥料 | |
| C. | 蜂蜡、沥青、玻璃都是非晶体 | |
| D. | 台秤、天平、弹簧测力计都是测量质量的工具 |
4.向一定质量的Zn和Fe的混合物中,加入一定质量的CuCl2溶液,充分反应后过滤,将滤渣洗涤、干燥后称量.质量没有发生变化,对所得滤液和滤渣有如下四种判断.其中判断正确的是( )
| A. | 滤液可能是无色的 | B. | 滤液中一定有ZnCl2和FeCl2 | ||
| C. | 滤渣中的物质可能有3种 | D. | 滤渣中加稀盐酸一定有气泡产生 |
11.下列关于燃烧与灭火的说法中,正确的是( )
| A. | 放在空气中的木桌椅没有燃烧,是因为桌椅不是可燃物 | |
| B. | 油锅着火,用锅盖盖灭,是为了降低可燃物的温度 | |
| C. | 防止森林大火蔓延,开挖隔离带,是为了将可燃物与火隔离 | |
| D. | 住房失火,消防队员用水扑灭,是为了降低可燃物的着火点 |
9.小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.
【探究目的】探究所得溶液的酸碱性;
【提出猜想】所得溶液可能呈碱性,也可能呈酸性,还可能呈中性.
【实验验证】
【分析与思考】
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:取样,加入金属锌,若现象为产生气泡,则所取溶液呈酸性;若无现象,则呈中性.
【探究目的】探究所得溶液的酸碱性;
【提出猜想】所得溶液可能呈碱性,也可能呈酸性,还可能呈中性.
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1~2mL,滴入1~2滴无色酚酞试液; | 无色酚酞溶液变红色 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈酸性或中性 |
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:取样,加入金属锌,若现象为产生气泡,则所取溶液呈酸性;若无现象,则呈中性.



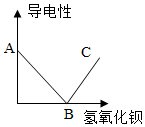 溶液具有导电性是因为溶液中存在着自由移动的离子,当接通电路时,这些自由移动的离子能定向移动,产生电流,而且在一定条件下,离子浓度越高,导电性就越强.某同学做了如下的实验:向硫酸溶液中逐渐滴加氢氧化钡溶液,并利用相应的仪器测定溶液的导电性,绘制如下的图.请回答下列的问题.
溶液具有导电性是因为溶液中存在着自由移动的离子,当接通电路时,这些自由移动的离子能定向移动,产生电流,而且在一定条件下,离子浓度越高,导电性就越强.某同学做了如下的实验:向硫酸溶液中逐渐滴加氢氧化钡溶液,并利用相应的仪器测定溶液的导电性,绘制如下的图.请回答下列的问题.