题目内容
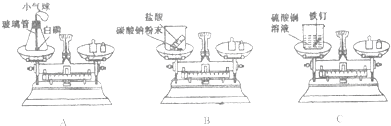
10.(1)如图,A、B、C三个实验用于验证质量守恒定律,其中不能达到实验目的是B,理由是生成的二氧化碳气体散逸到空气中去了[提示:Na2CO3+2HCl═2NaCl+H2O+CO2↑ Fe+CuSO4═FeSO4+Cu]
选取其中一个实验,提出改进思路.选取B一个实验,提出改进思路:在密闭容器中进行.
(2)用原子的观点解释质量守恒定律.化学反应过程中原子种类、原子数目、原子质量没变.
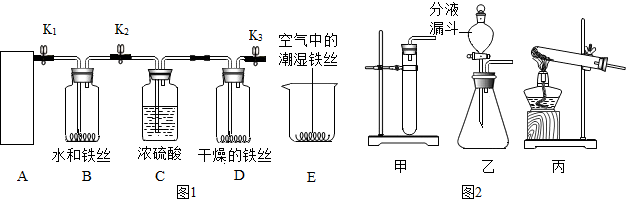
分析 做验证质量守恒定律的实验时所选用的装置应该考虑到:①如果反应物中有气体参加反应,或生成物中有气体生成,应该选用密闭装置.②如果反应物中没有气体参加生成物中也没有气体生成,装置可不考虑密闭.
化学反应的过程,就是参加反应的各物质(反应物)的分子破裂成原子,原子重新组合而生成其他物质分子的过程.此过程中原子本身没有任何变化,只是结合方式进行了重新的组合.
解答 解:(1)用图A中的装置进行验证质量守恒定律,能达到目的,原因在于装置是密封的.
图B不能达到目的,因为生成的二氧化碳气体散逸到空气中去了.
图C也能达到目的,因为生成物和反应物中都没有气体产生.
选取B一个实验,提出改进思路:在密闭容器中进行.
故填:B,生成的二氧化碳气体散逸到空气中去了;在密闭容器中进行.
(2)化学反应过程中原子种类、原子数目、原子质量没变,故遵守质量守恒定律.
故答案为:
(1)B,生成的二氧化碳气体散逸到空气中去了,选取B一个实验,提出改进思路:在密闭容器中进行.
(2)化学反应过程中原子种类、原子数目、原子质量没变
点评 本题主要考查了如何解释质量守恒定律的内容方面的知识,在做这种类型题目时,要求学生要注意总结规律,这样学习化学,可以达到事半功倍的效果.

练习册系列答案
相关题目
15.下列几种形状相同的金属和相同稀盐酸反应,产生气体速率最快的是( )
| A. | Mg | B. | Zn | C. | Fe | D. | Cu |
15.下列有关溶解度的说法,正确的是( )
| A. | 20℃时,100克水里溶解了20克某物质,则在20℃时,该物质的溶解度为20克 | |
| B. | 100克水中溶解40克物质刚好饱和,则该物质的溶解度为40克 | |
| C. | 50℃时,50克水中最多可溶解20克某物质,则100℃时该物质的溶解度为20克 | |
| D. | 20℃时,30克某物质中逐渐加入水,当加入100克水时,该物质恰好完全溶解,则20℃时该物质的溶解度为30克 |
2.现有一杯20℃时的氢氧化钙饱和溶液,对其进行如下操作,其中能使溶质质量分数保持不变是( )
| A. | 温度不变,加入少量的氢氧化钙固体 | |
| B. | 温度不变,往溶液中加入蒸馏水 | |
| C. | 往溶液中加入生石灰并恢复到20℃ | |
| D. | 升高温度 | |
| E. | 降低温度 | |
| F. | 往溶液中通入CO2气体 |
19. 钒被誉为“合金的维生素”,钒元素的相关信息如图,下列有关钒的说法正确的是( )
钒被誉为“合金的维生素”,钒元素的相关信息如图,下列有关钒的说法正确的是( )
 钒被誉为“合金的维生素”,钒元素的相关信息如图,下列有关钒的说法正确的是( )
钒被誉为“合金的维生素”,钒元素的相关信息如图,下列有关钒的说法正确的是( )| A. | 属于非金属元素 | B. | 原子核内中子数为23 | ||
| C. | 原子核外电子数为23 | D. | 相对原子质量为50.94g |