题目内容
15.小华利用铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液五种试剂,完成了验证铁、铜、银的金属活动顺序的实验.结束后,对该实验的废液进行探究.(1)通过观察,发现废液呈蓝色,则废液中一定含有硫酸铜.
(2)利用铁、铜、银的金属活动顺序,他分析出该废液中还一定含有硫酸亚铁.
(3)通过实验,他发现该废液中还含有硫酸.请写出利用题中所给的试剂证明废液中硫酸存在的化学方程式Fe+H2SO4═FeSO4+H2↑.
(4)小明同学另取少量废液,选用其它物质,利用中和反应原理,也证明了硫酸的存在.小明选择的物质是氢氧化钡溶液,现象为产生白色沉淀.
分析 硫酸铜溶液是蓝色的;
铁能和稀硫酸反应生成硫酸亚铁和氢气,能和硫酸铜反应生成硫酸亚铁和铜;
稀硫酸能和氢氧化钡反应生成白色沉淀硫酸钡和水,属于中和反应.
解答 解:(1)通过观察,发现废液呈蓝色,则废液中一定含有硫酸铜.
故填:硫酸铜.
(2)利用铁、铜、银的金属活动顺序,检验铁和铜的活动性顺序时,可以用铁、铜和稀硫酸相互混合,也可以用铁和硫酸铜混合,铁能和稀硫酸反应生成硫酸亚铁和氢气,能和硫酸铜反应生成硫酸亚铁和铜,因此该废液中还一定含有硫酸亚铁.
故填:硫酸亚铁.
(3)把铁丝伸入溶液中时,产生气泡,说明溶液中含有硫酸,反应的化学方程式为:Fe+H2SO4═FeSO4+H2↑.
故填:Fe+H2SO4═FeSO4+H2↑.
(4)小明选择的物质是氢氧化钡溶液,向溶液中加入氢氧化钡溶液时,如果产生白色沉淀,说明溶液中含有硫酸.
故填:氢氧化钡溶液;产生白色沉淀.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
5.1995年东京地铁发生沙林毒气事件,很多人中毒.它说明了构成物质的微粒( )
| A. | 可以再分 | B. | 在不停运动 | C. | 很少 | D. | 之间有间隔 |
6.某化合物一个分子X2O中电子数为10,则X的核电荷数为( )
| A. | 1 | B. | 2 | C. | 8 | D. | 5 |
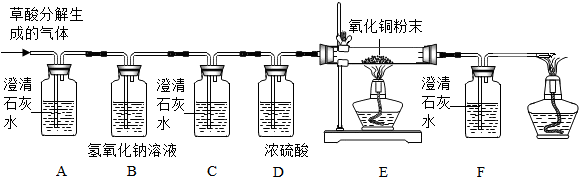
3.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水,某化学课外兴趣小组对生成物中碳的氧化物种类进行了如下实验探究
(1)【提出问题】生成物中有哪几种碳的氧化物?
(2)【提出猜测】
(3)【设计实验】基于猜测3,依据CO和CO2的性质,兴趣小组同学设计了如下实验:
(4)【实验探究】
①观察到A装置(填序号)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成;
②有两种实验现象都能分别证明草酸分解的气体中含有CO:
Ⅰ.C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊:
Ⅱ.E装置中出现黑色粉末变成红色粉末的现象;
(5)【实验结论】通过实验探究证明:猜测3成立:草酸分解的化学方程式是C2H2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O;
(6)【问题讨论】
①B装置的作用是检验二氧化碳是否被完全吸收,D装置的作用是吸收水分;
②装置末端酒精灯的作用是处理尾气CO.
(1)【提出问题】生成物中有哪几种碳的氧化物?
(2)【提出猜测】
| 猜测1 | 猜测2 | 猜测3 |
| 只有CO | 只有 CO2 | 含有CO和CO2 |
(4)【实验探究】
①观察到A装置(填序号)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成;
②有两种实验现象都能分别证明草酸分解的气体中含有CO:
Ⅰ.C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊:
Ⅱ.E装置中出现黑色粉末变成红色粉末的现象;
(5)【实验结论】通过实验探究证明:猜测3成立:草酸分解的化学方程式是C2H2O4$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+CO↑+H2O;
(6)【问题讨论】
①B装置的作用是检验二氧化碳是否被完全吸收,D装置的作用是吸收水分;
②装置末端酒精灯的作用是处理尾气CO.

