题目内容
16.某同学发现化肥袋上有一标签,如图1所示: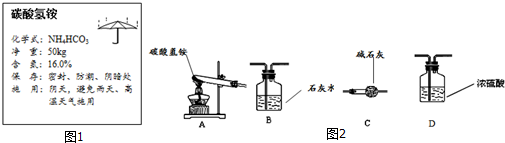
根据图示回答下列问题:
(1)碳酸氢铵是由4 种元素组成的,各元素的质量比N:H:C:O为14:5:12:48.
(2)写出碳酸氢铵的一点化学性质受热易分解.
【提出问题】
A.为什么要避免高温天气使用?
B.这种化肥含氮量是否达到16%,化肥中碳酸氢铵的含量是多少?
带着这些问题,她取了一些化肥样品,进入实验室.
【查找资料】
A.碱石灰能够吸收水和二氧化碳,但是不吸收氨气. B.浓硫酸能吸收氨气.
【性质实验探究】
她设计了如图2的实验装置:
(3)用A装置给碳酸氢铵加热,装药品前,她必须进行的一步操作是检查装置的气密性.
(4)取少量碳酸氢铵加入试管,加热,闻到刺激性气味,此气体化学式为NH3.
(5)连接A、B装置,继续加热,试管口出现小水珠,同时观察到B中的现象是变浑浊.
(6)碳酸氢铵在受热时发生反应的文字或符号表达式是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O.
【含量分析】
将装置A、C、D依次连接,加入10g化肥样品,加热至A中固体质量不再改变.
她称量装置D的质量如表:
| 实验前D装置的质量 | 150g |
| 实验后D装置的质量 | 151.7g |
(8)通过反应的表达式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮量为14%.(用百分数表示)
(9)请计算此化肥中碳酸氢铵的质量分数(表示写出计算过程).
分析 (1)根据化学式中元素组成考虑几种元素组成;依据元素的质量比等于各元素原子的相对原子质量和的比解答即可;
(2)根据化学性质是需要通过化学变化就表现出的性质进行解答;
(3)根据装药品前需要检查装置的气密性进行解答;
(4)根据碳酸氢铵受热分解生成氨气,氨气具有刺激性气味进行解答;
(5)根据碳酸氢铵受热分解生成氨气、二氧化碳和水进行解答;
(6)根据碳酸氢铵受热分解生成氨气、二氧化碳和水进行解答;
(7)根据碱石灰能吸收水和二氧化碳,浓硫酸和氨气反应生成硫酸铵进行解答;
(8)根据氨气的质量求出此化肥含氮量即可;
(9)根据氨气的质量求出碳酸氢铵的质量分数即可.
解答 解:(1)根据碳酸氢铵的化学式可知,它含有N、H、C、O四种元素;N、H、C、O元素的质量比为14:(1×5):12:(16×3)=14:5:12:48;
(2)碳酸氢铵的化学性质有:受热易分解;故填:受热易分解;
(3)装药品前需要检查装置的气密性;故填:检查装置的气密性;
(4)碳酸氢铵受热分解生成氨气,氨气具有刺激性气味,氨气的化学式为NH3;故填:NH3;
(5)碳酸氢铵受热分解生成氨气、二氧化碳和水,二氧化碳能使澄清石灰水变浑浊,所以观察到试管口的现象是有水珠出现,B中的现象是澄清石灰水变浑浊;故填:有水珠出现;澄清石灰水变浑浊;
(6)碳酸氢铵受热分解生成氨气、二氧化碳和水,反应的符号表达式是NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O;
(7)碱石灰能吸收水和二氧化碳,浓硫酸和氨气反应生成硫酸铵,所以实验后D装置增加的质量就是氨气的质量,所以氨气的质量为151.7g-150g=1.7g;氮元素的质量为=1.7g×$\frac{14}{17}$×100%=1.4g;
(8)此化肥含氮量=$\frac{1.4g}{10g}$×100%=14%;
(9)设碳酸氢铵的质量为x.
NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O
79 17
x 1.7g
$\frac{79}{x}=\frac{17}{1.7g}$
x=7.9g
化肥中碳酸氢铵的质量分数$\frac{7.9g}{10g}$×100%=79%.
故答案为:(1)4;14:5:12:48;
(2)受热易分解;
(3)检查装置的气密性;
(4)NH3;
(5)变浑浊;
(6)NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O;
(7)1.7g;1.4g;
(8)14%;
(9)79%.
点评 解答本题要充分理解标签中提供的信息,并根据物质的性质的区分方法,从而得出正确的结论.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案| A. |  天然气燃烧 | B. |  冰雪融化 | C. |  葡萄酿酒 | D. |  光合作用 |
| A. | 原子是化学变化中最小的粒子,所以原子不能再分 | |
| B. | 分子、原子可以构成物质,所以物质一定是由分子、原子构成的 | |
| C. | 水是由氢元素和氧元素组成的,所以由氢元素和氧元素组成的物质一定是水 | |
| D. | 化合物是含有不同种元素的纯净物,所以由不同种元素组成的纯净物一定是化合物 |
| 物质名称 | 物质组成 (用化学式表示) | 构成物质的微粒 (用符号表示) | 物质中各元素的质量比 |
| 氧气 | O2 | ||
| 过氧化氢 | mH:mO=1:l6 | ||
| 熟石灰 | Ca(OH)2 |