题目内容
19.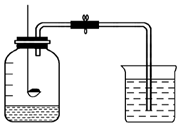 已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:(1)实验中红磷要过量,其目的是全部消耗掉集气瓶中内的氧气.
(2)加紧弹簧夹,在空气中点燃红磷,并迅速深入集气瓶中,塞紧橡皮塞,此时观察到的主要现象是红磷燃烧,产生了大量的白烟,反应的文字表达式是红磷+氧气$\stackrel{点燃}{→}$五氧化二磷(用字母表达亦可).
(3)待燃烧停止,白烟消失并冷却至室温后,打开弹簧夹,观察到的现象是烧杯中的水进入集气瓶,水倒流入集气瓶中的体积约占集气瓶剩余体积的$\frac{1}{5}$,出现该现象的原因是红磷燃烧消耗了氧气,氧气约占空气体积的$\frac{1}{5}$.
(4)若实验中测得氧气的体积分数小雨$\frac{1}{5}$,则造成这种误差的可能原因有哪些?(至少写三种)
①红磷的量不足;②装置漏气;③未等到装置冷却到室温就打开了弹簧夹.
(5)从该实验中还可推知氮气的那些性质?是写出其中的两种:
①氮气难溶于水;②氮气不燃烧、不支持燃烧.
分析 本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
解答 解:(1)红磷在氧气中燃烧生成五氧化二磷.该实验中红磷稍过量,目的是全部消耗掉集气瓶中内的氧气;
(2)加紧弹簧夹,在空气中点燃红磷,并迅速深入集气瓶中,塞紧橡皮塞,此时观察到的主要现象是红磷燃烧,产生了大量的白烟,反应的文字表达式是:红磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(3)待燃烧停止,白烟消失并冷却至室温后,打开弹簧夹,观察到的现象是:烧杯中的水进入集气瓶,水倒流入集气瓶中的体积约占集气瓶剩余体积的$\frac{1}{5}$,出现该现象的原因是 红磷燃烧消耗了氧气,氧气约占空气体积的$\frac{1}{5}$.
(4)若实验中测得氧气的体积分数小于$\frac{1}{5}$,则造成这种误差的可能原因有:①红磷的量不足;②装置漏气;③未等到装置冷却到室温就打开了弹簧夹.
(5)从该实验中水倒流入集气瓶中的体积只有的$\frac{1}{5}$而未充满整个集气瓶,说明了氮气是难溶于水的;红磷燃烧一会熄灭了,说明氮气不燃烧不支持燃烧,其化学性质不活泼;
答案:(1)全部消耗掉集气瓶中内的氧气.(2)红磷燃烧,产生了大量的白烟;红磷+氧气$\stackrel{点燃}{→}$五氧化二磷.(3)烧杯中的水进入集气瓶,水倒流入集气瓶中的体积约占集气瓶剩余体积的$\frac{1}{5}$,红磷燃烧消耗了氧气,氧气约占空气体积的$\frac{1}{5}$,(4)①红磷的量不足;②装置漏气;③未等到装置冷却到室温就打开了弹簧夹.(5)难溶于水的;不燃烧不支持燃烧.
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

 名校课堂系列答案
名校课堂系列答案| A. | 测定是否有毒 | B. | 用燃着的木条 | C. | 闻气味 | D. | 用澄清石灰水 |
| A. | 山洪暴发 | B. | 泥石流 | C. | 桥下烧烤 | D. | 打伞嬉戏 |
| A. | 该物质的一个分子中含25个原子 | |
| B. | 该物质中碳、氢、钾、氧元素之间的质量比是6:7:3:8 | |
| C. | 该物质的相对分子质量为324g | |
| D. | 该物质是由碳、氢、钾、氧四种元素组成的 |
(1)a.蒸馏水 b.镁条 c.水银 d.碳酸氢钠 e.氢氧化钡溶液 f.碘
属于单质的是bcf;属于氧化物的是a;属于化合物的是ad;属于混合物的是e.
(2)在一密闭容器中有M、N、P、Q四种物质,在一定条件下使之充分反应后,测得反应前后各物质的质量如下表所示:
| 物质 | M | N | P | Q |
| 反应前的质量/g | 80 | 1 | 1 | 1 |
| 反应前的质量/g | 1 | 待测 | 45 | 19 |
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
②N的待测值为18g.
| 物 质 | 所含杂质 | 除去杂质的方法 | |
| A | CO2气体 | CO | 点燃 |
| B | KClO3 | KCl | 加热至不再产生气体 |
| C | Fe粉 | Cu粉 | 加入足量稀硫酸,充分反应,过滤 |
| D | FeSO4溶液 | CuSO4 | 加入足量铁粉,充分反应,过滤 |
| A. | A | B. | B | C. | C | D. | D |