题目内容
8.已知镁条在点燃条件下,与氧气可以化合,与氮气也可以化合,与二氧化碳则发生置换反应,将镁条在空气中点燃,理论上可发生的化学反应方程式为①2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO②3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2③2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C实验测得产物中主要为氧化镁含少量氮化镁,没有碳单质,试说明原因O2的活泼性最强,N2次之,CO2最弱,因此先与O2反应,再与N2反应,最后和CO2反应,实验中Mg的量不足,故测得产物中主要为氧化镁含少量氮化镁,没有碳单质.
分析 根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;结合物质的活动性分析.
解答 解:镁条被点燃在空气中燃烧与氧气生成氧化镁,反应的化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;镁与氮气反应生成氧化镁,反应的化学方程式为:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;金属镁能在二氧化碳气体中燃烧生成碳和氧化镁,故答案为:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;O2的活泼性最强,N2次之,CO2最弱,因此先与O2反应,再与N2反应,最后和CO2反应,实验中Mg的量不足,故测得产物中主要为氧化镁含少量氮化镁,没有碳单质.
故答案为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;O2的活泼性最强,N2次之,CO2最弱,因此先与O2反应,再与N2反应,最后和CO2反应,实验中Mg的量不足,故测得产物中主要为氧化镁含少量氮化镁,没有碳单质.
点评 本题难度不是很大,主要考查了有关的化学方程式的书写,从而加强学生对有关知识的掌握.

练习册系列答案
相关题目
18.通过下列图示实验得出的结论中不正确的是( )
| A | B | C | D |
 |  | 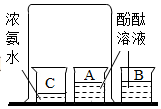 | 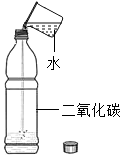 |
| 既说明甲烷具有可燃性,又说明甲烷中含有碳、氢两种元素 | 既说明二氧化碳密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧 | 既说明分子在不断的运动,又说明氨分子能使酚酞试液变红 | 既说明二氧化碳溶于水,又说明二氧化碳能与水反应 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
19.下列实验方案及现象与结论一致的是( )
| A | B | C | D | |
| 方案 |  | 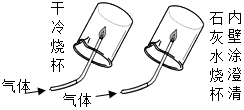 |  | 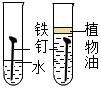 |
| 现象 | 热水中未燃烧的白磷在通入氧气后燃烧 | 点燃某气体后,干冷烧杯内壁出现无色液滴,澄清石灰水变浑浊 | 黄铜片能在铜片上刻画出痕迹 | 水中的铁钉生锈,植物油中的铁钉没生锈 |
| 结论 | 燃烧需要氧气 | 该气体就是甲烷(CH4) | 合金的硬度比组成它的纯金属小 | 铁生锈只需要与氧气接触 |
| A. | A | B. | B | C. | C | D. | D |
16.蛋白质是构成细胞的基本物质,是机体生长及修补受损组织的主要原料.下列食物中属于糖类的是( )
| A. |  米饭 | B. |  红烧肉 | C. |  鲫鱼 | D. |  西红柿 |
17.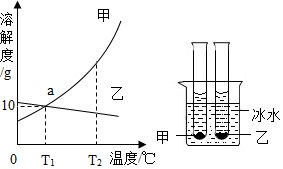 甲、乙两种固体的溶解度曲线如图.现将两试管分别装有甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体)放进盛有冰水的烧杯里,则下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图.现将两试管分别装有甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体)放进盛有冰水的烧杯里,则下列说法正确的是( )
 甲、乙两种固体的溶解度曲线如图.现将两试管分别装有甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体)放进盛有冰水的烧杯里,则下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图.现将两试管分别装有甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体)放进盛有冰水的烧杯里,则下列说法正确的是( )| A. | a点表示甲乙两物质的溶解度相等且都为10克 | |
| B. | 放入盛有冰水的烧杯后,试管里甲乙两溶液中的溶质都减少 | |
| C. | T1℃时,甲乙两溶液的溶质质量分数都为10% | |
| D. | 甲仍为饱和溶液,乙可能为不饱和溶液 |
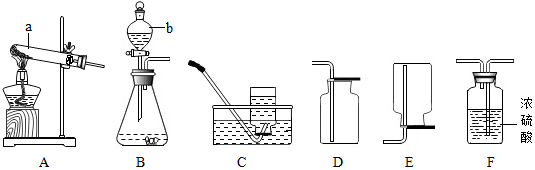
18.下列实验操作正确的是( )
| A. | 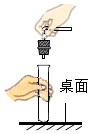 塞进橡皮塞 | B. | 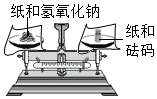 称取一定质量的氢氧化钠固体 | ||
| C. | 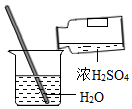 稀释浓硫酸 | D. | 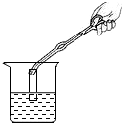 测定溶液的pH |