题目内容
19.(1)铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图.
①铁锅含有合金单质Fe(填化学式),含有的有机合成材料是塑料.
②炒菜时铁锅中的油着火可用锅盖盖灭,其原理是隔绝氧气.
③铝锅轻便、耐用,其原因是:密度小且铝的表面易形成致密的氧化铝保护膜.
④废旧铁锅、铝锅不要随意丢弃,应回收利用,这样做的意义是节约金属资源.
(2)氯化钡是一种可溶性重金属盐,广泛应用于化工领域,用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如下:

①毒重石要进行粉碎的目的是增大与盐酸的接触面积;气体X的化学式为CO2.
②操作Y的名称是过滤,滤液2中可循环利用的物质除水外还有氯化钡.洗涤氯化钡制品最适宜的洗涤剂是C(填字母).
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
③滤渣水洗的目的是溶解含有的氯化钡.
(3)A、B、C、D、E是初中化学常见的物质,它们之间的转化关系如图甲所示,部分反应条件、反应物及生成物已略去.图乙所示的是A、B、C、D、E的相关信息(重叠部分表示两种物质的共同点).请回答下列问题:

Ⅰ.A的化学式为Fe2O3.
Ⅱ.反应②的基本反应类型为置换反应.
Ⅲ.物质E的用途之一为高能燃料.
Ⅳ.反应④的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
分析 根据已有的金属的性质进行分析解答,增大反应物的接触面积能促进反应的进行;在饱和溶液中不能再溶解这种物质;根据框图提供的信息结合已有的物质的性质推断,据此解答.
解答 解:(1)①铁锅含有合金单质是铁,含有的有机合成材料是塑料,故填:Fe,塑料.
②炒菜时铁锅中的油着火可用锅盖盖灭能起到隔绝氧气的作用,故填:隔绝氧气.
③铝锅轻便是因为密度小,耐用是因为铝的表面易形成致密的氧化铝保护膜,故填:密度小且铝的表面易形成致密的氧化铝保护膜.
④废旧铁锅、铝锅应回收利用的意义是节约金属资源、保护环境,故填:节约金属资源.
(2)①毒重石要进行粉碎能增大与盐酸的接触面积;碳酸钡与盐酸反应生成的气体X是二氧化碳,其化学式为CO2,故填:增大与盐酸的接触面积,CO2.
②经过操作Y得到了晶体好滤液,故操作Y的名称是过滤,滤液2中含有氯化钡,可循环利用的物质除水外还有氯化钡.洗涤氯化钡制品最适宜的洗涤剂是30℃饱和氯化钡溶液,因为不能再溶解氯化钡,但是可以溶解其他的杂质,故填:过滤,氯化钡,C;
③滤渣水洗能溶解含有的氯化钡,故填:溶解含有的氯化钡.
(3)据图可以看出,A和B含有相同的元素,且A是红色的,B是黑色的,故A可能是氧化铁,B可能是四氧化三铁;氧化铁能反应生成铁,铁能燃烧生成四氧化三铁,故C是铁,E是气体单质,氧化铁与E反应生成铁,故E是氢气,铁能生成固体单质D,故D可能是铜,带入框图,推断合理;
Ⅰ.A是氧化铁,故填:Fe2O3.
Ⅱ.反应②是铁与硫酸铜溶液反应生成硫酸亚铁和铜,属于基本反应类型中的置换反应,故填:置换反应.
Ⅲ.物质E是氢气,据有可燃性,可以用作高能燃料,故填:高能燃料.
Ⅳ.反应④是铁在氧气中燃烧生成四氧化三铁,故填:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
点评 本题考查的是金属的有关性质和应用,完成此题,可以依据已有的金属的性质进行即可.

| A. | 给试管加热之前要先预热 | |
| B. | 用50 mL的量筒量取5.55 mL的氯化钠溶液 | |
| C. | 将氢氧化钠固体直接放在托盘天平的托盘上称量 | |
| D. | 用pH试纸直接浸入溶液中测溶液的pH |
| A. |  加热液体 | B. |  点燃酒精灯 | C. |  添加酒精 | D. |  熄灭酒精灯 |
| A. | 2NH4+:二个铵根离子 | |
| B. | H2O:一个水分子中含有一个氢分子 | |
| C. | Mg2+:一个镁离子带二个单位的正电荷 | |
| D. | $\stackrel{+2}{Cu}$O:氧化铜中铜元素的化合价为正二价 |
【活动与探究一】用对比实验方法探究二氧化碳的性质.
| 实验一 | 实验二 |
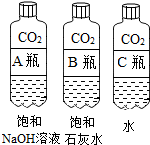 | 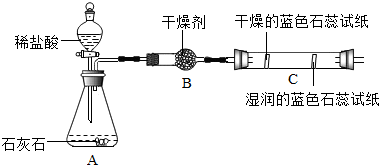 |
(2)实验二观察到C装置中发生的现象是干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色,结论是CO2+H2O=H2CO3(用化学方程式表示).
【活动与探究二】用变量控制方法探究影响物质溶解性的因素.
| 实验三 | 实验四 |
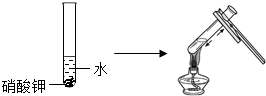 | 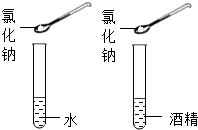 |
【活动与探究三】定量测定空气中氧气的含量.
| 实验五 | |
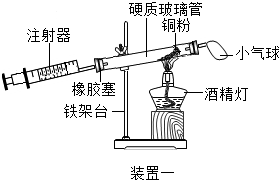 | 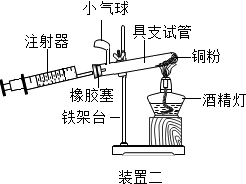 |
根据下表提供的实验数据,完成下表:
| 硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
| 30mL | 20mL | 12mL | 16% |
| A. | 去超市购物,用布质购物袋 | B. | 网上购买大量闲置物品 | ||
| C. | 节假日随父母出游,经常开私家车 | D. | 外出就餐,超量点菜 |

