题目内容
9.一定量的锌和氧化锌的混合物中锌元素的质量分数为65%,取10g加入足量的稀硫酸溶液,再向溶液中加入足量的氢氧化钠溶液,得到沉淀的质量为( )| A. | 10g | B. | 9.9g | C. | 6.5g | D. | 8g |
分析 根据锌元素的质量结合氢氧化锌中锌元素的质量分数求出氢氧化锌的质量
解答 解:锌与氧化锌与足量稀硫酸反应,生成了硫酸锌,再向所得溶液中滴加足量的氢氧化钠溶液,硫酸锌与氢氧化钠溶液反应生成了氢氧化锌,在化学反应中锌元素质量不变,故混合物中锌元素的质量就是氢氧化锌中锌元素的质量;故氢氧化锌的质量:$\frac{10g×65%}{\frac{65}{99}×100%}$=9.9g;
故选:B.
点评 根据化学方程式计算以及元素质量守恒法计算是化学计算中最重要的两种计算方法.

练习册系列答案
相关题目
20. CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.
CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.
【查阅资料】
①通常情况下,1体积水溶解1体积的CO2. ②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生.
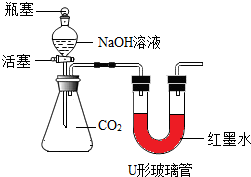
【实验探究】小红同学设计了如图所示的实验装置(锥形瓶内充满CO2),并进行实验.
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管左侧的红墨水液面升高(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,写出CO2与NaOH溶液反应的化学方程式:2NaOH+CO2=Na2CO3+H2O;
【反思与评价1】小明认为小红的实验方案不严密,理由是二氧化碳溶于水(或与水发生反应)也会使锥形瓶内气压减小;
【拓展实验】兴趣小组的同学们为此又设计了下表所示的两种方法,进一步探究.请填写表中的空格.
【反思与评价2】同学们经过讨论,认为拓展实验的方法一(填“方法一”或“方法二”)依然不严密,理由是CaCl2+2NaOH=Ca(OH)2↓+2NaCl.
 CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.
CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.【查阅资料】
①通常情况下,1体积水溶解1体积的CO2. ②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生.
【实验探究】小红同学设计了如图所示的实验装置(锥形瓶内充满CO2),并进行实验.
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管左侧的红墨水液面升高(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,写出CO2与NaOH溶液反应的化学方程式:2NaOH+CO2=Na2CO3+H2O;
【反思与评价1】小明认为小红的实验方案不严密,理由是二氧化碳溶于水(或与水发生反应)也会使锥形瓶内气压减小;
【拓展实验】兴趣小组的同学们为此又设计了下表所示的两种方法,进一步探究.请填写表中的空格.
| 实验方法 | 操作过程 | 现象 | 实验结论 |
| 方法一 | 取小红实验后锥形瓶内的溶液适量,加入足量CaCl2溶液 | 有白色沉淀生成 | CO2与NaOH发生了反应 |
| 方法二 | 取小红实验后锥形瓶内的溶液适量,加入足量稀硫酸 | 有气泡冒出 |
17.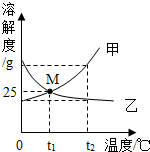 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的( )
 如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的( )
如图为甲、乙两物质(均不含结晶水)的溶解度曲线,下列说法错误的( )| A. | 乙的饱和溶液由t2℃降温到t1℃时,溶质的质量分数不变 | |
| B. | 甲中含有少量乙,可以用冷却热饱和溶液的方法提纯甲 | |
| C. | t1℃时,50g水中分别加入25g的甲、乙,均可得到75g的饱和溶液 | |
| D. | t1℃时,等质量甲、乙两物质的饱和溶液蒸发等质量的水,所得溶液中溶质的质量一定相等 |
