题目内容
12. 向100g硫酸铜溶液中,逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:
向100g硫酸铜溶液中,逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题:(1)将A点所对应的混合物过滤,滤液中所含溶质为硫酸钠;
(2)图中A点所对应的溶液总质量为200g;
(3)求(1)中所得滤液的溶质质量分数(请写出计算过程).
分析 (1)由图示和题意可知,A点为硫酸铜溶液和NaOH溶液恰好完全反应,故滤液中所含溶质为硫酸钠;
(2)根据质量守恒定律反应前溶液质量和减去沉淀质量即为A点所对应的溶液总质量;
(3)结合化学方程式由沉淀质量即可计算出所得滤液的溶质硫酸钠质量,即可解答.
解答 解:(1)A点为硫酸铜溶液和NaOH溶液恰好完全反应,故滤液中所含溶质为硫酸钠;答案:硫酸钠;
(2)A点所对应的溶液总质量为100g+109.8g-9.8g=200g;答案:200;
(3)(1)中所得滤液的溶质质量为x,
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
98 142
9.8g x
$\frac{98}{9.8g}=\frac{142}{x}$
x=14.2g
(1)中所得滤液的溶质质量分数:$\frac{14.2g}{200g}×$100%=7.1%.
答:(1)中所得滤液的溶质质量分数7.1%.
点评 本题是根据化学方程式与溶液结合一道综合计算题,会从题目中获取信息是正确解决本题的关键.

练习册系列答案
相关题目
20.下列关于自然界中的水的说法正确的是( )
| A. | 地球上的淡水资源取之不尽,用之不竭 | |
| B. | 水体污染的来源主要有工业污染、农业污染和生活污染 | |
| C. | 水分解可以得到氢气,因此水是廉价且清洁的能源物质 | |
| D. | 水的软化是将海水变成可饮用的淡水 |
7. 为了验证镁、铜两种金属活动性大小,某同学设计了如图所示的实验,为了达到试验目的,溶液应该选择( )
为了验证镁、铜两种金属活动性大小,某同学设计了如图所示的实验,为了达到试验目的,溶液应该选择( )
 为了验证镁、铜两种金属活动性大小,某同学设计了如图所示的实验,为了达到试验目的,溶液应该选择( )
为了验证镁、铜两种金属活动性大小,某同学设计了如图所示的实验,为了达到试验目的,溶液应该选择( )| A. | 稀硫酸 | B. | 硫酸镁溶液 | C. | 氯化钠溶液 | D. | 植物油 |
17.正确的化学实验操作是实验成功的重要保证.下列实验操作正确的是( )
| A. | 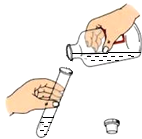 倾倒液体 | B. | 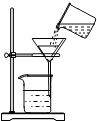 过滤 | ||
| C. |  检查气密性 | D. | 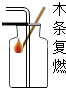 检验氧气是否收集满 |
4.酸、碱、盐在工农业生产和日常生活中应用广泛.下列做法错误的是( )
| A. | 用石灰乳与硫酸铜溶液配制农药波尔多液 | |
| B. | 用稀盐酸除去铁制品表面的铁锈 | |
| C. | 用食盐水除去水壶中的水垢 | |
| D. | 施用复合肥硝酸钾能使作物枝叶繁茂,并增加抗倒伏能力 |
1.铁生锈探秘

为探究铁生锈的原因,化学兴趣小组的同学进行了如图所示的四个实验,实验结果显示:B、D实验中铁生了锈,而A、C实验中没有明显的现象,仔细分析这4 个实验,回答下列问题:
(1)评价方案
对照实验指除了一个变量外,其他的量都保持不变的实验.该实验方案中采用了对照实验方法.请指出其中的对照实验(填ABCD实验代号)和变量.
第①组对照实验AB,变量水分.
第②组对照实验BC,变量氧气.
第③组对照实验BD,变量食盐.
(2)解释数据
实验时,每隔一段时间测量导管内水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度/cm )
导致B、D实验装置中导管内水面上升的原因是铁丝生锈吸收了空气中的氧气.
(3)获得结论
根据本实验,你认为导致铁生锈的物质有水和氧气;能加快铁生锈的物质是食盐.

为探究铁生锈的原因,化学兴趣小组的同学进行了如图所示的四个实验,实验结果显示:B、D实验中铁生了锈,而A、C实验中没有明显的现象,仔细分析这4 个实验,回答下列问题:
(1)评价方案
对照实验指除了一个变量外,其他的量都保持不变的实验.该实验方案中采用了对照实验方法.请指出其中的对照实验(填ABCD实验代号)和变量.
第①组对照实验AB,变量水分.
第②组对照实验BC,变量氧气.
第③组对照实验BD,变量食盐.
(2)解释数据
实验时,每隔一段时间测量导管内水面上升的高度,结果如下表所示(表中所列数据为导管中水面上升的高度/cm )
| 时间/小时 编号 | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| C | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| D | 0 | 0.4 | 1.2 | 3.4 | 7.6 | 9.5 | 9.8 |
(3)获得结论
根据本实验,你认为导致铁生锈的物质有水和氧气;能加快铁生锈的物质是食盐.
2.硝酸钾在不同的溶解度数据如表,下列说法错误的是( )
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| A. | 硝酸钾的溶解度受温度影响变化较大 | |
| B. | 60℃时,饱和硝酸钾溶液中溶质与溶液质量之比为11:21 | |
| C. | 20℃时,10g水中加入5g硝酸钾充分溶解后再加入5g水,前后溶质的质量分数不变 | |
| D. | 将溶质质量分数为28%的硝酸钾溶液从60℃降温至20℃,没有晶体析出 |
 如图是某胃药标签的部分内容.小明同学测定该药品中NaHCO3含量的过程如下:取10粒该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5克.称得反应后烧杯内物质的总质量为64.3克.
如图是某胃药标签的部分内容.小明同学测定该药品中NaHCO3含量的过程如下:取10粒该药剂研碎后放入烧杯中,加入50克水后充分搅拌,再向其中滴加稀盐酸至溶液的pH=7时(已知药品中的其它成分既不溶于水,也不与稀盐酸反应),形成NaCl的不饱和溶液,共消耗稀盐酸11.5克.称得反应后烧杯内物质的总质量为64.3克.