题目内容
有13.5克氯化铜样品,当它与足量硝酸银溶液反应后得到氯化银29克,则样品中可能混有的盐是( )
| A、氯化钡 | B、氯化汞 |
| C、氯化锌 | D、氯化镁 |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:先假设13.5g全部是氯化铜,根据化学方程式计算出生成沉淀的质量,如果实际生成的沉淀质量>假设13.5g全部是氯化铜时生成的沉淀质量,则说明杂质物质中氯元素的质量分数要大于氯化铜中氯元素的质量分数.
解答:解:假设13.5g全部是氯化铜,设生成沉淀的质量为x,
CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2
135 287
13.5g x
135:287=13.5g:x
解之得:x=28.7g.
由计算可知,实际生成的沉淀29g>假设13.5g全部是氯化铜时生成的沉淀28.7g.
如果多生成沉淀的话,则应该样品中的Cl的离子数应该是比纯的CuCl2含有的Cl离子数多,相同质量的物质中含有的离子多的话,应该是杂质中含氯离子的那个物质的相对分子质量应该比铜小.因此可以这么说杂质中的氯元素的质量分数比CuCl2中氯元素的质量分数大.观察选项可知,只有氯化镁中的氯元素的质量分数比CuCl2中氯元素的质量分数大.
故选D.
CuCl2+2AgNO3=2AgCl↓+Cu(NO3)2
135 287
13.5g x
135:287=13.5g:x
解之得:x=28.7g.
由计算可知,实际生成的沉淀29g>假设13.5g全部是氯化铜时生成的沉淀28.7g.
如果多生成沉淀的话,则应该样品中的Cl的离子数应该是比纯的CuCl2含有的Cl离子数多,相同质量的物质中含有的离子多的话,应该是杂质中含氯离子的那个物质的相对分子质量应该比铜小.因此可以这么说杂质中的氯元素的质量分数比CuCl2中氯元素的质量分数大.观察选项可知,只有氯化镁中的氯元素的质量分数比CuCl2中氯元素的质量分数大.
故选D.
点评:本题主要考查学生灵活运用化学方程式和元素的质量分数解答问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
下列对实验现象的描述不正确的是( )
| A、硫在空气中燃烧发出微弱淡蓝色火焰 |
| B、铝在氧气中燃烧发出耀眼白光 |
| C、将金属银投入到稀盐酸中,银表面产生大量气泡 |
| D、硫酸铜溶液中滴加氢氧化钠溶液产生蓝色沉淀 |
下列各组物质的分类正确的是( )
| A、合金、涤纶、塑料都是合成材料 |
| B、铜、水银和食盐水都是导体 |
| C、一氧化碳、乙醇和聚乙烯都是有机物 |
| D、氮气、海水和五氧化二磷都是纯净物 |
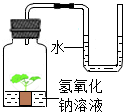 如图所示,将一盆绿色植物放在-个密闭的装有氢氧化钠溶液的容器内,玻璃导管的一端插入密闭容器,另一端经胶皮管与U形管相连;U形管中装有-定量的水,将此装置放在黑暗中24小时后,U形管中液面的变化情况( )
如图所示,将一盆绿色植物放在-个密闭的装有氢氧化钠溶液的容器内,玻璃导管的一端插入密闭容器,另一端经胶皮管与U形管相连;U形管中装有-定量的水,将此装置放在黑暗中24小时后,U形管中液面的变化情况( )| A、不变 | B、左侧液面上升 |
| C、右侧液面上升 | D、无法确定 |
下列各物质中,属于合成材料的是( )
| A、陶瓷 | B、钢筋混凝土 |
| C、生铁 | D、聚乙烯塑料 |
下列叙述中正确的是( )
| A、被雨水淋湿的自行车,先用油抹布擦,再用干抹布擦 |
| B、在已生锈的金属防盗门表面上直接涂漆,防止进一步生锈 |
| C、在水龙头上镀锌、镀铬是为了防止金属生锈 |
| D、在手表的表壳上镀铜,是因为铜不生锈且美观 |
下列各组物质能大量共存于水溶液中的是( )
| A、CuSO4和KOH |
| B、Ba(NO3)2 和Na2CO3 |
| C、CaCl2和Zn(N03)2 |
| D、HCl和AgNO3 |
下列各组物质中,前者是单质,后者是化合物的是( )
| A、空气,氯化钾 |
| B、液氧,二氧化碳 |
| C、钢,氧化铁 |
| D、过氧化氢,水蒸气 |
下列变化中,加入盐酸能进一步实现的是( )
| A、Fe→FeCl3 |
| B、Na2SO4→NaCl |
| C、CuO→CuCl2 |
| D、CaCO3→CO2 |