题目内容
13.近几年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤而形成的,此外,各种机动车排放的尾气也是形成酸雨的重要原因.【提出问题】通过实验证明煤中含有碳元素和硫元素.
【查阅资料】(1)“二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),该反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4”.
(2)“二氧化硫和二氧化碳一样,也能使澄清石灰水变浑浊.”请写出二氧化硫与澄清石灰水反应的化学方程式:SO2+Ca(OH)2═CaSO3↓+H2O.
根据上述资料,甲同学、乙同学和丙同学分别设计实验方案进行探究.
【实验探究】(3)甲同学:
“实验操作”:甲同学进行了如下图所示A、B两步实验:
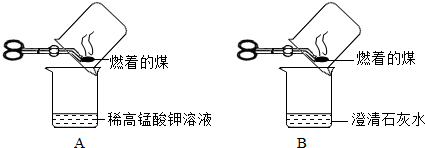
“实验现象”:A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊.
“得出结论”:煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素.
(4)乙同学认为甲同学的实验方案不合理,其理由是:因为二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素.
(5)丙同学:
“实验操作”:丙同学进行了如下图所示实验(部分装置在图中略去):
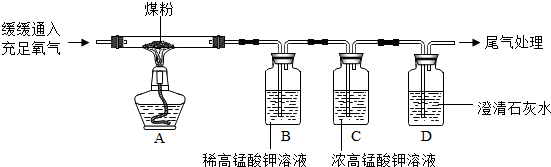
【探究与结论】(6)上图C装置的作用是除去二氧化硫并检验二氧化硫是否除尽.
(7)要证明煤中含有碳元素和硫元素,丙同学的实验中现象是B中溶液褪色,C中溶液仍为紫红色,D中溶液变浑浊.
分析 本题以实验探究的形式,检验煤的碳元素和硫元素,需要我们知道质量守恒定律;会书写化学反应式;了解试验装置的合理性;会分析各种试验现象.
解答 解:[查阅资料](2)二氧化硫能使澄清石灰水变浑浊,一定生成了沉淀物CaSO3.故化学反应式为:SO2+Ca(OH)2═CaSO3↓+H2O;
故答案为:SO2+Ca(OH)2═CaSO3↓+H2O;
(4)据资料知,A试验中的稀高锰酸钾溶液褪色,说明煤中含硫元素.B试验中的澄清石灰水变浑浊,说明煤中可能含有碳元素也可能含有硫元素.故不合理.
故答案为:因为二氧化硫也会使澄清石灰水变浑浊,无法证明煤中含有碳元素.
(6)二氧化硫能使高锰酸钾溶液褪色(由紫红色变为无色),故B装置的作用是:检验二氧化硫;浓高锰酸钾溶液可与二氧化硫反应除去二氧化硫,高锰酸钾溶液又可检验二氧化硫的存在.故C装置的作用是:除去二氧化硫并检验二氧化硫是否除尽.
故答案是:除去二氧化硫并检验二氧化硫是否除尽.
(7)观察现象:加热碳粉生成二氧化硫,二氧化硫与稀高锰酸钾溶液反应并使其褪色.二氧化硫在B中已与高锰酸钾溶液反应,C中的浓高锰酸钾溶液仍为紫红色.煤粉燃烧生成的二氧化碳可使澄清石灰水变浑浊.
故答案是:B中溶液褪色,C中溶液仍为紫红色,D中溶液变浑浊.
点评 本题以实验探究的形式,检验物质的存在和物质的性质.培养了学生的动手能力和动脑思考的能力.

练习册系列答案
相关题目
3.小明在厨房里看到一种白色固体,他认为“可能是食盐”.对于“可能是食盐”,应该是科学探究中的( )
| A. | 提出问题 | B. | 猜想与假设 | C. | 进行实验 | D. | 获得结论 |
8.实验中除杂的思路有两种:一是将杂质除去,二是将有用物质提取出来,以下除杂方法与后者的思路一致的是( )
| A. | 实验室用蒸馏的方法制取蒸馏水 | |
| B. | 用灼热的铜网除去N2中混有的少量O2 | |
| C. | 加热蒸发法除去氯化钠溶液中混有的少量盐酸 | |
| D. | 用过滤的方法从双氧水制氧气剩余废液中回收二氧化锰 |
18.下列变化属于化学变化的是( )
| A. | 木材制成桌椅 | |
| B. | 矿石粉碎 | |
| C. | 酒精挥发 | |
| D. | 二氧化碳气体通入澄清石灰水,石灰水变浑浊 |
 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: