题目内容
4.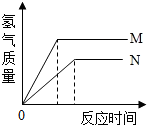 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )
等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是( )| A. | 生成H2的质量M<N | B. | 相对原子质量较大的是N | ||
| C. | 产生H2的速率N>M | D. | M、N两种金属中较活泼的是N |
分析 A、根据图中数据可以判断生成氢气的质量;
B、根据反应的化学方程式及其金属的质量、生成氢气的质量可以判断金属相对原子质量的大小;
C、根据氢气中的氢元素来自于稀盐酸,因此根据生成氢气的质量可以判断消耗稀盐酸的质量;
D、金属越活泼,与稀盐酸反应的速率越快.
解答 解:A、由图中信息可知,M与稀盐酸反应生成氢气的质量大,故A错误;
B、设M、N的质量都是z,相对原子质量为x、y,生成氢气的质量为m、n,
M+2HCl═MCl2+H2↑,N+2HCl═NCl2+H2↑,
x 2 y 2
z m z n
x=$\frac{2z}{m}$,y=$\frac{2z}{n}$,
因为m>n,所以x<y,即N的相对原子质量大于M的相对原子质量,故B正确;
C、由图中信息可知,M与稀盐酸反应生成氢气的速率快于N和稀盐酸反应生成氢气的速率,故C错误;
D、由图中信息可知,M与稀盐酸反应的速率快,说明M比N活泼,故D错误.
故选:B.
点评 由图中信息可知,反应需要的时间越短,说明反应速率越快,反应需要的时间越长,说明反应速率越慢,要注意理解.

练习册系列答案
相关题目
14.下列物质中,前者属于纯净物、后者属于混合物的是( )
| A. | 水和冰混合、澄清石灰水 | B. | 净化后的空气、氧化镁 | ||
| C. | 生锈的铁钉、液氧 | D. | 氧化铜、氧化镁 |
12.如图化学实验基本操作图示正确的是( )
| A. | 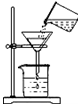 过滤 | B. | 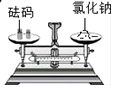 称取氯化钠 | C. |  稀释浓硫酸 | D. | 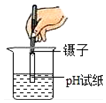 测溶液pH |
19.现有质量分数为98%的浓硫酸100g,将上述浓硫酸稀释成质量分数为20%的稀硫酸.需要加入水的质量是多少( )
| A. | 290g | B. | 400g | C. | 390g | D. | 500g |
16.一些食物的近似pH如表:
下列说法中错误的是( )
| 食物 | 葡萄汁 | 苹果汁 | 牛奶 | 鸡蛋清 |
| pH | 3.5~4.5 | 2.9~3.3 | 6.3~6.6 | 7.6~8.0 |
| A. | 鸡蛋清和牛奶显碱性 | B. | 苹果汁和葡萄汁显酸性 | ||
| C. | 苹果汁比葡萄汁酸性强 | D. | 胃酸过多的人应少饮葡萄汁 |
13.为确定铜、铁、银的金属活泼性强弱,用下列试剂可直接完全实现的是( )
| A. | 硝酸银溶液、铁片、铜片 | B. | 硝酸铜溶液、硝酸银溶液、铁片 | ||
| C. | 铜片、硝酸亚铁溶液、硝酸银溶液 | D. | 铁片、稀盐酸、银片、铜片 |
4.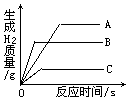 将质量相等的A、B、C三种金属(颗粒大小相同),同时分别放入三份溶质质量分数 相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论错误的是.(已知:A、B、C在生成物中均为+2价)( )
将质量相等的A、B、C三种金属(颗粒大小相同),同时分别放入三份溶质质量分数 相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论错误的是.(已知:A、B、C在生成物中均为+2价)( )
 将质量相等的A、B、C三种金属(颗粒大小相同),同时分别放入三份溶质质量分数 相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论错误的是.(已知:A、B、C在生成物中均为+2价)( )
将质量相等的A、B、C三种金属(颗粒大小相同),同时分别放入三份溶质质量分数 相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论错误的是.(已知:A、B、C在生成物中均为+2价)( )| A. | 放出H2的质量是A>B>C | B. | 金属活动性顺序是B>A>C | ||
| C. | 反应速率最大的是B | D. | 相对原子质量是B>C>A |