题目内容
7.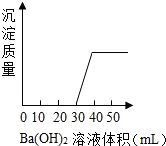 有一混合物是由盐酸、碳酸钠、硫酸、氯化铜、硝酸钾五种物质中的一种或几种混合而成.向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.据此回答:
有一混合物是由盐酸、碳酸钠、硫酸、氯化铜、硝酸钾五种物质中的一种或几种混合而成.向该混合溶液中滴入Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.据此回答:该混合溶液中一定含有盐酸和氯化铜,可能含有硝酸钾.
分析 根据物质的性质、产生沉淀的质量与加入Ba(OH)2溶液体积的关系分析判断.若混合溶液有硫酸,滴入氢氧化钡应立即出现白色沉淀,排除硫酸;盐酸与碳酸钾不能共存,排除碳酸钾;进行解答本题.
解答 解:由于硫酸与氢氧化钡反应生成了硫酸钡沉淀,若混合溶液有硫酸,滴入氢氧化钡应立即出现白色沉淀,排除硫酸;由于开始时加入的氢氧化钡不产生沉淀,说明了含有盐酸,加入一定量时产生了沉淀,说明了含有氯化铜;由于盐酸能与碳酸钠不能共存,说明了不能存在碳酸钠;通过以上实验不能判断硝酸钾是否存在,是可能含有的物质.
故答为:盐酸和氯化铜 硝酸钾.
点评 本题的难度不大,了解常见物质的性质和反应的现象是解答本题的基础知识.

练习册系列答案
相关题目
18.将下列物质的浓溶液加入鸡蛋清溶液中,不能使蛋白质失去活性的是( )
| A. | 硫酸铵 | B. | 乙酸铅 | C. | 甲醛 | D. | 浓硝酸 |
2.科学兴趣小组的同学们对蛋壳的成分开展了有关探究.同学们的实验过程如下:
①将一定量的蛋壳放入容器中;②往其中加入适量的稀盐酸,观察到有较多的气泡产生;③…;④得出结论:蛋壳的主要成分是碳酸盐.
(1)请补全第③步的实验内容与现象将收集的气体通入澄清的石灰水,澄清的石灰水变浑浊.
(2)为了测定蛋壳中碳酸钙的质量分数,同学们用蛋壳与足量的稀盐酸充分反应,得到有关数据如表:(CO2的密度为2克/升)
请你通过列式计算蛋壳中碳酸钙的质量分数.
①将一定量的蛋壳放入容器中;②往其中加入适量的稀盐酸,观察到有较多的气泡产生;③…;④得出结论:蛋壳的主要成分是碳酸盐.
(1)请补全第③步的实验内容与现象将收集的气体通入澄清的石灰水,澄清的石灰水变浑浊.
(2)为了测定蛋壳中碳酸钙的质量分数,同学们用蛋壳与足量的稀盐酸充分反应,得到有关数据如表:(CO2的密度为2克/升)
| 蛋壳的质量(克) | 加入稀盐酸质量(克) | 收集到CO2气体体积(升) |
| 7.5 | 100 | 1.1 |
12.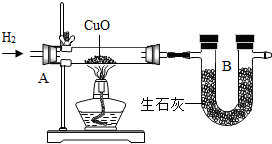 为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验,通过称量反应前后装置A、B的质量,结果测得m(H):m(O)>1:8,比理论值偏高,其原因不可能是( )
为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验,通过称量反应前后装置A、B的质量,结果测得m(H):m(O)>1:8,比理论值偏高,其原因不可能是( )
 为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验,通过称量反应前后装置A、B的质量,结果测得m(H):m(O)>1:8,比理论值偏高,其原因不可能是( )
为了进一步测定水中的元素组成的质量比,某科技小组的同学设计了下列实验,通过称量反应前后装置A、B的质量,结果测得m(H):m(O)>1:8,比理论值偏高,其原因不可能是( )| A. | 通入的氢气未经过净化干燥 | |
| B. | 装置A内管口有水凝结 | |
| C. | 氧化铜没有完全还原 | |
| D. | 装置B同时吸收了空气中的水蒸气和CO2 |
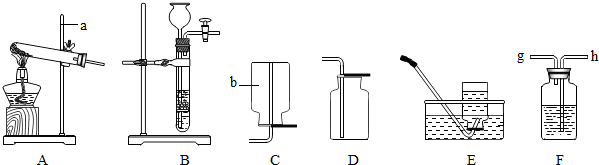
16.利用下列装置能达到相应实验目的是( )
| A. |  分离KNO3和NaCl | B. | 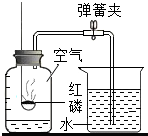 测定空气中O2含量 | ||
| C. | 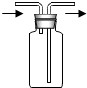 收集CO2气体 | D. |  用氢气还原氧化铜 |
17.无论是石灰水中的水,还是蒸馏水中的水,只要是水,化学式是( )
| A. | 不一样 | B. | 一样H2O | C. | 可能不一样 | D. | 不知道 |
 如图是常见气体的分子模型图,其中“●”和“○”分别代表二种原子模型.已知气体A可在气体B中燃烧生成气体C,且气体C能通过稀盐酸与石灰石反应产生.
如图是常见气体的分子模型图,其中“●”和“○”分别代表二种原子模型.已知气体A可在气体B中燃烧生成气体C,且气体C能通过稀盐酸与石灰石反应产生.