题目内容
16.根据如图提供的信息,请回答问题:
(1)A中铝原子的核电荷数为13,铝元素的相对原子质量为26.98.
(2)C在化学反应中易失(填“得”或“失”)电子达到稳定结构,若F为某元素的
原子,则m为7.
(3)属于同种元素的是BC(填字母);表示阴离子的是E(填字母).
(4)B和E两种粒子构成化合物的化学式为Na2S.
(5)相同质量的钠和铝两种金属,所含原子较多的是钠.
分析 (1)根据元素周期表的信息来分析;
(2)根据最外层电子数来分析;
(3)根据元素的概念以及离子的判断方法来分析;
(4)根据化合物的化学式写法来分析;
(5)同质量的金属,原子数最多即原子质量最小,因为原子的原子量与其质量是成正比关系,所以原子量最小的即是原子个数最多的金属.
解答 解:(1)由元素周期表信息可知,铝的核电荷数为13,相对原子质量为26.98;故填:13,26.98.
(2)C的最外层有1个电子,在化学反应中易失去一个电子;在原子中,质子数=核外电子数,X=17-2-8=7;故填:失,7.
(3)同种元素的粒子具有相同的质子数,B的核内质子数为11,C粒子的核内质子数为11,B与C属于同种元素.E中质子数<核外电子数,是阴离子;故填:BC,E.
(4)B是钠元素,E是硫元素,二者组成的化合物是硫化钠,故填:Na2S.
(5)元素的原子量与其真实质量成正比,由于原子量的大小关系是钠<铝,所以真实质量也是这一关系,故相同质量的2种金属含原子的多少关系是:钠>铝.
故填:钠.
点评 本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.完成下列有关物质的分类网络,并在括号内填上下列物质的类别名称.
①空气 ②氧气 ③高锰酸钾 ④铁粉 ⑤海水 ⑥二氧化锰 ⑦二氧化碳 ⑧氯酸钾.
| 物质(按所含物质种类 多少分) | 混合物 | 如:食盐水、混凝土 | ||
纯净物(按所含元素种类多少分) | 单质 | 如:氧气、氢气 | ||
| 化合物 | 氧化物 | 如MgO、CaO | ||
| 其他 | 如HCl、NaCl | |||
7.如图是元素周期表中的一格,从中获得的信息正确的是( )


| A. | 该元素原子的质子数为14 | B. | 该元素属于金属元素 | ||
| C. | 该元素是地壳中含量最多的元素 | D. | 该元素的相对原子质量为28.09g |
4.绿茶中的单宁酸(化学式为C76H52O46)具有抑制血压上升、清热解毒、抗癌等功效,下列说法错误的是( )
| A. | 单宁酸属于化合物 | |
| B. | 单宁酸由碳、氢、氧三种元素组成 | |
| C. | 单宁酸分子的相对分子质量为1700g | |
| D. | 一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 |
1.某兴趣小组同学对实验室制备氧气的条件进行如下探究.
【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的金属氧化物是氧化铜.
设计并完成实验】Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ.将X g氯酸钾与1.0g氧化铜均匀混合加热
实验现象分析】Ⅲ中X的值应为3.0g,实验Ⅰ和Ⅲ比较可证明CuO改变KClO3分解的速率.将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同,这些步骤是为了证明氧化铜在该化学反应前后质量和化学性质都不变.
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的符号表达式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
【实验反思】实验Ⅱ和Ⅲ对比的目的是CuO对KClO3催化效果是否比MnO2好.
【提出问题】②MnO2的用量对 H2O2分解反应有何影响?
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3%H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计.)
【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出过氧化氢的用量越多,产生的氧气越多.

(2)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线.曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求.在此实验条件下,若MnO2的质量有4克(一药匙),就能使如图C(填字母)烧杯中所装的3%H2O2溶液,其分解速度最接近实验要求.

【提出问题】①氧化铜是否也能做氯酸钾分解的催化剂?它是否比二氧化锰催化效果好?
【查阅资料】研究表明,许多金属氧化物对氯酸钾的分解有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
| 催化剂 温度/℃ 反应程度 | 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 |
| 开始反应 | 420 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |
设计并完成实验】Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ.将X g氯酸钾与1.0g氧化铜均匀混合加热
实验现象分析】Ⅲ中X的值应为3.0g,实验Ⅰ和Ⅲ比较可证明CuO改变KClO3分解的速率.将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同,这些步骤是为了证明氧化铜在该化学反应前后质量和化学性质都不变.
【结论】氧化铜也能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应的符号表达式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
【实验反思】实验Ⅱ和Ⅲ对比的目的是CuO对KClO3催化效果是否比MnO2好.
【提出问题】②MnO2的用量对 H2O2分解反应有何影响?
【设计并完成实验】利用图甲装置探究“MnO2的用量对 H2O2分解反应的影响”,实验中为3%H2O2溶液,装置中产生氧气的量可以用压强传感器测出(在等温条件下,产生氧气体积与装置内压强成正比,反应放热忽略不计.)
【讨论交流】(1)图乙是“0.1克MnO2与不同体积的3%H2O2溶液混合”的实验结果,从图中可以看出过氧化氢的用量越多,产生的氧气越多.

(2)当用“3%H2O2溶液8毫升与不同质量的MnO2混合”时,得到如图丙所示的曲线.曲线的斜率显示,当MnO2的用量增加到0.08克时,分解速度达到实验要求.在此实验条件下,若MnO2的质量有4克(一药匙),就能使如图C(填字母)烧杯中所装的3%H2O2溶液,其分解速度最接近实验要求.

 氢能是21世纪最理想的能源,但制氢还没有想出真正合适的方法,图是电解水制氢的简易装置图.回答下列问题:
氢能是21世纪最理想的能源,但制氢还没有想出真正合适的方法,图是电解水制氢的简易装置图.回答下列问题: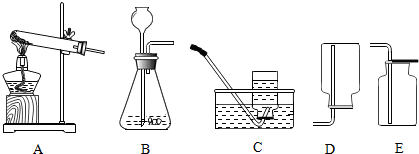

 表示碘元素的原子(填“原子”、“阳离子”或“阴离子”)结构示意图.由图可知,碘元素应位于元素周期表中的第5周期.
表示碘元素的原子(填“原子”、“阳离子”或“阴离子”)结构示意图.由图可知,碘元素应位于元素周期表中的第5周期.