题目内容
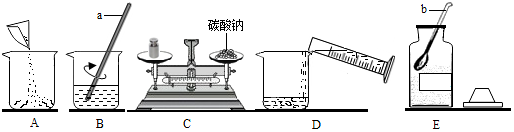
3.在实验室里,下列物质的制备原理错误的是( )| A. | 用铜与稀硫酸反应制硫酸铜 | |
| B. | 用石灰石与稀盐酸反应制二氧化碳 | |
| C. | 加热氯酸钾与二氧化锰的混合物制氧气 | |
| D. | 用氢气还原灼热的氧化铜制铜 |
分析 A、铜不能和稀硫酸反应;
B、实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
C、氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气;
D、高温条件下,氧化铜和氢气反应生成铜和水.
解答 解:A、铜不能和稀硫酸反应,因此不能用铜与稀硫酸反应制硫酸铜;
B、实验室中可以用石灰石与稀盐酸反应制二氧化碳;
C、实验室中可以用加热氯酸钾与二氧化锰的混合物制氧气;
D、实验室中可以用氢气还原灼热的氧化铜制铜.
故选:A.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
13.如图是过滤器的制作和过滤装置图,则下列有关说法错误的是( )
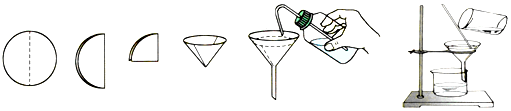

| A. | 图中制过滤器时加水湿润,是为了使滤纸能紧贴漏斗内壁 | |
| B. | 过滤时,待滤液不能高于滤纸的边缘 | |
| C. | 过滤后的液体中可能会溶有可溶性物质 | |
| D. | 过滤时,为了加快过滤速度,可用玻璃棒在漏斗内搅拌 |
14.下列与实验相关的叙述正确的是( )
| A. | 浓硫酸溅到手上,应立即用水冲洗 | |
| B. | 将无色酚酞滴入某溶液后呈红色,说明该溶液呈碱性 | |
| C. | 用pH试纸测定某溶液的pH值,应将玻璃棒在蒸馏水中清洗后再取待测液测定 | |
| D. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
11.下列说法中正确的是( )
| A. | 中和反应有盐和水生成,所以有盐和水生成的化学反应一定是中和反应 | |
| B. | 单质只含一种元素,所以含一种元素的物质一定是单质 | |
| C. | 离子是带电的原子或原子团,所以带电的微粒一定是离子 | |
| D. | 淀粉遇到碘水呈蓝色,所以与碘水作用呈现蓝色的物质中含有淀粉 |
18.只有一种物质就能将稀硫酸、水、澄清石灰水三种无色液体鉴别出来,可供选用的物质是:①pH试纸、②酚酞试液、③稀盐酸、④碳酸钠溶液、⑤石蕊试液,其中能用于鉴别的是( )
| A. | ①④⑤ | B. | ①②⑤ | C. | ①②③ | D. | ③④⑤ |
15.下列是某同学利用实验室的器材进行实验,设计了四种实验方案你认为可行的是( )
| A. | 用过滤的方法分离NaCl和NaNO3的混合物 | |
| B. | 用稀硫酸除去氧化铁中混有的少量氢氧化铁 | |
| C. | 采用高温煅烧碳酸钙来制取氧化钙 | |
| D. | 用稀盐酸除去混在铜粉中的氧化铜粉末 |