题目内容
有一包固体样品,可能是碳酸钠、硫酸铜、氢氧化钠、氯化钡中的一种或几种.为探究其成分,李老师取用一定量样品,加水溶解,过滤得到白色沉淀甲和无色滤液乙.
【探究活动一】自主小组探究白色沉淀甲的成分.
【探究活动二】合作小组探究固体样品中是否含有氢氧化钠,设计了如下实验:
【反思】实验步骤2中加入过量试剂的目的是 .
【结论】通过两个小组的共同探究,得出了原固体样品中含有的成分.
【探究活动一】自主小组探究白色沉淀甲的成分.
| 实验操作 | 实验现象 | 结论 |
| 取白色沉淀甲,滴加足量的稀盐酸 | 沉淀消失 | 白色沉淀甲中一定含有 |
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取无色滤液乙,加入碳酸钠溶液 | 无明显现象 | 无色滤液乙中一定不含氯化钡 |
| 2 | 取适量无色滤液乙,加入过量的 |
生成白色沉淀 | 无色溶液中一定含有碳酸钠 |
| 3 | 取实验步骤2中的滤液,滴加 |
原固体样品中一定存在氢氧化钠 |
【结论】通过两个小组的共同探究,得出了原固体样品中含有的成分.
考点:物质的鉴别、推断,盐的化学性质
专题:混合物组成的推断题
分析:硫酸钡是一种不溶于水的白色沉淀,碳酸钠和氯化钡反应能够生成白色沉淀碳酸钡;硫酸钡一般不溶于水、酸、碱,碳酸钡不溶于水,溶于酸;
玻璃棒的作用有:引流、搅拌、转移物质等;
根据实验现象可以判断物质的存在情况.
玻璃棒的作用有:引流、搅拌、转移物质等;
根据实验现象可以判断物质的存在情况.
解答:解:【探究活动一】
滴加足量的稀硝酸时,沉淀消失,说明沉淀中没有硫酸钡,只有反应生成的碳酸钡.
故填:碳酸钡.
【探究活动二】根据碳酸钠溶液能和氯化钙溶液反应生成碳酸钙白色沉淀,氢氧化钠溶液呈碱性,能使酚酞溶液变红变红,所以实验方案为:
故填:氯化钙;无色酚酞;溶液变红
【反思】实验步骤2中加入过量试剂的目的是除去滤液中的碳酸钠,排除干扰.故填:除去滤液中的碳酸钠,排除干扰.
滴加足量的稀硝酸时,沉淀消失,说明沉淀中没有硫酸钡,只有反应生成的碳酸钡.
故填:碳酸钡.
【探究活动二】根据碳酸钠溶液能和氯化钙溶液反应生成碳酸钙白色沉淀,氢氧化钠溶液呈碱性,能使酚酞溶液变红变红,所以实验方案为:
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取无色滤液乙,加入碳酸钠溶液 | 无明显现象 | 无色滤液乙中一定不含氯化钡 |
| 2 | 取适量无色滤液乙,加入过量的氯化钙溶液,过滤 | 生成白色沉淀 | 无色溶液中一定含有碳酸钠 |
| 3 | 取实验步骤2中的滤液,滴加无色酚酞溶液 | 溶液变红 | 原固体样品中一定存在氢氧化钠 |
【反思】实验步骤2中加入过量试剂的目的是除去滤液中的碳酸钠,排除干扰.故填:除去滤液中的碳酸钠,排除干扰.
点评:根据实验现象进行判断时,要对硫酸钡和碳酸钡的溶解性有一个全面的理解,硫酸钡一般不溶于水、酸和碱,而碳酸钡属于碳酸盐,溶于酸.

练习册系列答案
相关题目
用如图所示能够使气球先膨胀,过一段时间又恢复到原状的一组固体和液体是( )
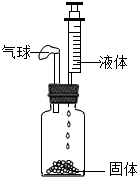

| A、固体:硝酸铵;液体:水 |
| B、固体:氢氧化钠;液体:水 |
| C、固体:碳酸钠;液体:稀盐酸 |
| D、固体:氯化钠;液体:水 |
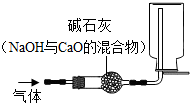 我们熟悉的几种气体,①H2 ②O2 ③CO2 ④SO2 ⑤CH4,其中可用如图所示装置干燥并收集的是(省略了铁架台等仪器) ( )
我们熟悉的几种气体,①H2 ②O2 ③CO2 ④SO2 ⑤CH4,其中可用如图所示装置干燥并收集的是(省略了铁架台等仪器) ( )| A、①② | B、③④ | C、①⑤ | D、①②⑤ |
如图中“○”和“●”分别表示不同元素的原子,则其中表示化合物的是( )
A、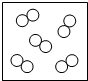 |
B、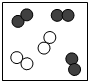 |
C、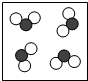 |
D、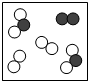 |
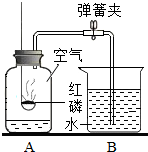 如图是测定空气中氧气含量的实验.请回答问题:A中红磷燃烧的现象是
如图是测定空气中氧气含量的实验.请回答问题:A中红磷燃烧的现象是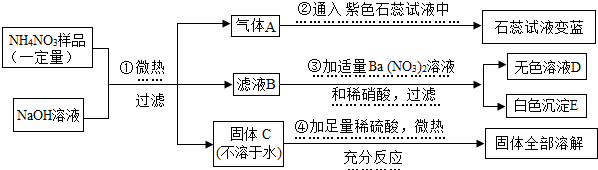

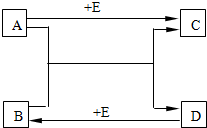 已知A、B、C、D、E是初中化学常见的物质,它们相互转化关系如图:
已知A、B、C、D、E是初中化学常见的物质,它们相互转化关系如图: