题目内容
20.请选择适当的物质填空(填字母).A.生石灰 B.熟石灰C.石灰石 D.氢氧化铝 E.浓硫酸 F.聚乙烯
(1)可作食品干燥剂的是A.
(2)可作食品包装材料的是F.
(3)可中和胃酸过多的是D.
(4)常用于改良酸性土壤的是B.
(5)用于实验室制取二氧化碳的是C.
分析 (1)生石灰吸水常用作干燥剂;
(2)聚乙烯是塑料的主要成分,可以制成食品包装袋,
(3)考虑胃酸的主要成分为稀盐酸,利用酸碱中和反应;
(4)酸性土壤一般用碱性物质来中和;
(5)考虑实验室制取二氧化碳的反应原理.
解答 解:(1)生石灰吸水常用作干燥剂;
(2)聚乙烯是塑料的主要成分,可以制成食品包装袋,
(3)因为胃酸的主要成分为稀盐酸,故可中和胃酸过多的是氢氧化铝;
(4)熟石灰的主要成分是氢氧化钙,是一种碱性的物质,可用于中和酸性土壤改良土壤结构;
(5)用于实验室制取二氧化碳的是石灰石.
故选:(1)A;(2)F;(3)D;(4)B;(5)C
点评 本题主要考查了常见物质的用途,在平时的学习中要注意知识的积累加强对物质性质的理解与应用,要明确物质的用途是由其性质决定的.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
15.下列物质露置于空气中,由于发生化学变化而使质量增加的是( )
| A. | 浓盐酸 | B. | 氯化钠 | C. | 浓硫酸 | D. | 氢氧化钠 |
5.下列物质中,属于纯净物的是( )
| A. | 无尘空气 | B. | 加碘食盐 | C. | 液态氧气 | D. | 武德合金 |
12.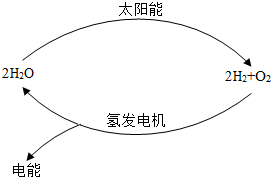 如图是一种最理想的氢能源循环体系,下列说法不正确的是( )
如图是一种最理想的氢能源循环体系,下列说法不正确的是( )
 如图是一种最理想的氢能源循环体系,下列说法不正确的是( )
如图是一种最理想的氢能源循环体系,下列说法不正确的是( )| A. | 该氢能源循环体系能实现将太阳能转化为电能 | |
| B. | 此循环中发生了反应:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | |
| C. | 该过程的实现,将解决能源危机和环境污染问题 | |
| D. | 目前化学家急需解决的问题是寻找合适的光照条件下分解水的催化剂 |
9.下列日常生活用品不能与水形成溶液的是( )
| A. | 食盐 | B. | 蔗糖 | C. | 白醋 | D. | 面粉 |
17.最近,3D打印公司Industry和著名自行车厂商TiCycles合作利用3D打印技术制造出全球首辆完整的钛金属自行车“Solid”.工业制取钛的过程中会发生如下变化:2FeTiO3+7Cl2+6C=2TiCl4+2FeCl3+6X,下列关于该反应的说法不正确的是( )
| A. | X的化学式为CO | B. | FeCl3溶于水,溶液呈浅绿色 | ||
| C. | C在该反应中表现出还原性 | D. | X可以用于从铁矿石中冶炼铁 |