题目内容
15.A~J都是初中化学中的常见物质,其中D、E对维持自然界生命活动至关重要,A、B为黑色固体,C是红色金属单质,H为气体.它们的相互转化关系如图所示,请回答下列问题: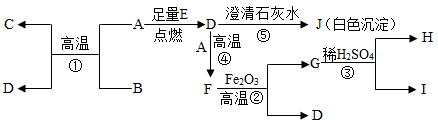
(1)写出下列物质的化学式:BCuO;IFeSO4.
(2)反应①②③④⑤中属于置换反应的为①③(填序号).
(3)写出反应②的化学方程式:3CO+Fe2O3 $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 根据题干提供的信息进行分析解答,A、B为黑色固体,C是红色金属单质,若A和B是碳和氧化铜的反应,C是铜,生成的D是二氧化碳,二氧化碳能使澄清的石灰水变浑浊,J是碳酸钙;由于碳在足量的氧气中燃烧生成了二氧化碳,则A是碳;E是氧气;二氧化碳能与碳高温反应生成一氧化碳,F是一氧化碳;一氧化碳还原氧化铁高温反应生成铁和二氧化碳,所以G是铁,铁与硫酸反应生成的H是氢气,I是硫酸亚铁,带入框图进行验证.据此解答.
解答 解:由题意可知,A、B为黑色固体,C是红色金属单质,若A和B是碳和氧化铜的反应,C是铜,生成的D是二氧化碳,二氧化碳能使澄清的石灰水变浑浊,J是碳酸钙;由于碳在足量的氧气中燃烧生成了二氧化碳,则A是碳;E是氧气;二氧化碳能与碳高温反应生成一氧化碳,F是一氧化碳;一氧化碳还原氧化铁高温反应生成铁和二氧化碳,所以G是铁,铁与硫酸反应生成的H是氢气,I是硫酸亚铁,带入框图,推断合理;
(1)由上述分析可知,B是CuO,I是FeSO4;
(2)①是碳与氧化铜反应生成铜和二氧化碳,属于置换反应,③是铁与硫酸反应生成硫酸亚铁和氢气,属于置换反应,④是碳与二氧化碳高温反应生成一氧化碳,属于化合反应,⑤是二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,不属于基本反应类型,所以属于置换反应的是:①③;
(3)②是一氧化碳与氧化铁高温反应生成铁和二氧化碳,反应的化学方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故答为:(1)CuO,FeSO4;(2)①③;(3)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的实验
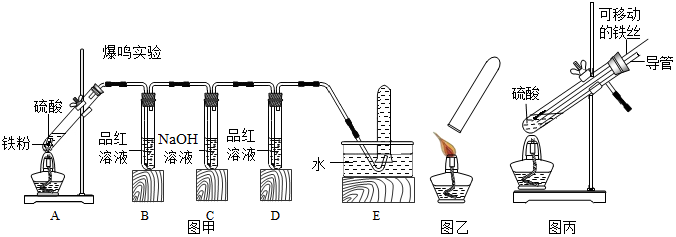
请帮助小明完成下表:
| A中硫酸的浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | ① | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ② |
| 实验三 | 25% | ③ | 不褪色 | ④ | 只有H2 |
【交流反思】(1)写出实验三中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑,
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】小明又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因防止生成的气体从导管逸出
,该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸.
| A. | 分子 | B. | 阳离子 | C. | 阴离子 | D. | 原子 |
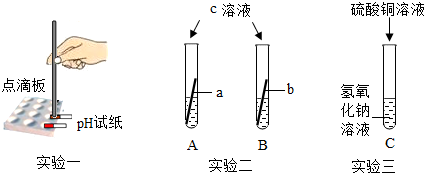
| A. | 甲溶液呈中性,乙溶液呈碱性 | |
| B. | 甲溶液属于酸性溶液,乙溶液属于碱性溶液 | |
| C. | 甲溶液一定是酸性溶液,乙溶液一定是碱性溶液 | |
| D. | 甲溶液使无色酚酞变红色,乙溶液不能使无色酚酞变色 |
| A. | NH4NO3 | B. | KNO3 | C. | (NH4)2HPO4 | D. | Ca(H2PO4)2 |
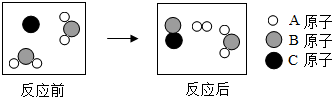 如图是某化学反应的微观示意图,该反应的基本类型是置换反应,生成物中A元素的化合价为0.
如图是某化学反应的微观示意图,该反应的基本类型是置换反应,生成物中A元素的化合价为0.