题目内容
 “前不久,有媒体报道,太原一名14岁的中学生,吃完零食后将食品干燥剂放进保温杯了,随后保温杯发生爆炸,导致其双眼严重受伤…”针对这则消息,化学小组的同学找来这种干燥剂(如图)到化学实验室进行研究.按要求填空.
“前不久,有媒体报道,太原一名14岁的中学生,吃完零食后将食品干燥剂放进保温杯了,随后保温杯发生爆炸,导致其双眼严重受伤…”针对这则消息,化学小组的同学找来这种干燥剂(如图)到化学实验室进行研究.按要求填空.【探究一】干燥剂的成分是什么?
同学们阅读干燥剂说明,上面写着“干燥剂,主要成分为生石灰,不可食用、不可浸水、不可开袋、不可玩耍”.则该物质做干燥剂的化学原理是
【探究二】保温杯爆炸的原因是什么?
甲同学向烧杯中加入一定量的水,将干燥剂倒入水中,发现烧杯中的水开始“沸腾”,并有白色的水蒸气冒出.由此可知生石灰遇水后会
结论:生石灰遇水放出大量的热量,使保温杯内压强增大引起爆炸,并且氢氧化钙具有腐蚀性,导致眼睛受伤.
【探究三】乙同学对甲同学实验后烧杯内的混合物产生了兴趣,并按下列步骤进行了实验:
①将烧杯中的混合物过滤,得到白色沉淀和滤液.过滤需要的仪器及用品是
②测定上述滤液的酸碱度,测定的方法是
【探究四】丙同学对上述乙同学过滤出的白色沉淀的成分提出了以下假设:
假设1:Ca(OH)2和CaCO3的混合物;假设2:只有CaCO3;假设3:只有Ca(OH)2;
为了判断几种假设的合理性,该同学继续进行试验,请你完成下列填空:
| 实验方案 | 实验现象 | 结论 |
| ①取少量沉淀放在一支试管中,加少量水振荡、静置后,滴入酚酞溶液 | | 假设2不成立 |
| ② | | 假设3不成立 |
【事件反思】同学们查阅资料发现,硅胶是一种高微孔结构的二氧化硅,无毒、无味、化学性质稳定,是一种安全绿色的干燥剂.因此同学们向有关部门建议用硅胶替代石灰做食品干燥剂.写出二氧化硅的化学式,并在化学式中标出硅元素的化合价
考点:食品干燥剂、保鲜剂和真空包装的成分探究,过滤的原理、方法及其应用,溶液的酸碱度测定,生石灰的性质与用途,碱的化学性质,盐的化学性质,有关元素化合价的计算,物质发生化学变化时的能量变化,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【探究一】生石灰与水反应会生成熟石灰;
【探究二】根据题干信息来分析反应过程的热量变化情况;
【探究三】过滤操作需要用到铁架台(带铁圈)、烧杯、漏斗、玻璃棒、滤纸等;测定溶液的酸碱度选用pH试纸,根据测定溶液pH的方法进行叙述;
【探究四】根据氢氧化钙溶液显碱性,碳酸钙与稀盐酸反应生成气体来进行分析;
【事件反思】根据常见元素的化合价和化合价的规定来分析解答.
【探究二】根据题干信息来分析反应过程的热量变化情况;
【探究三】过滤操作需要用到铁架台(带铁圈)、烧杯、漏斗、玻璃棒、滤纸等;测定溶液的酸碱度选用pH试纸,根据测定溶液pH的方法进行叙述;
【探究四】根据氢氧化钙溶液显碱性,碳酸钙与稀盐酸反应生成气体来进行分析;
【事件反思】根据常见元素的化合价和化合价的规定来分析解答.
解答:解:【探究一】氧化钙与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2;
【探究二】干燥剂放入水中,导致水沸腾,说明该反应放出热量;
【探究三】过滤操作需要用到铁架台(带铁圈)、烧杯、漏斗、玻璃棒、滤纸等;测定溶液的酸碱度是可用玻璃棒蘸取待测液体,点在pH试纸上,并与标准比色卡对照,得到pH;
【探究四】若假设②不成立,说明混合物中有氢氧化钙,其水溶液显碱性,加入无色酚酞试液,会看到变红色;若假设③不成立,说明混合物中还有碳酸钙,加入稀盐酸后会产生二氧化碳气体;碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;
【事件反思】在化合物中,氧元素显-2价,则二氧化硅中硅元素显+4价.
故答案为:【探究一】CaO+H2O=Ca(OH)2;
【探究二】放热;
【探究三】烧杯、玻璃棒、漏斗、铁架台(铁圈)、滤纸;用玻璃棒蘸取待测液体,点在pH试纸上,并与标准比色卡对照,得到pH.
【探究四】CaCO3+2HCl=CaCl2+H2O+CO2↑;
【事件反思】
O2.
【探究二】干燥剂放入水中,导致水沸腾,说明该反应放出热量;
【探究三】过滤操作需要用到铁架台(带铁圈)、烧杯、漏斗、玻璃棒、滤纸等;测定溶液的酸碱度是可用玻璃棒蘸取待测液体,点在pH试纸上,并与标准比色卡对照,得到pH;
【探究四】若假设②不成立,说明混合物中有氢氧化钙,其水溶液显碱性,加入无色酚酞试液,会看到变红色;若假设③不成立,说明混合物中还有碳酸钙,加入稀盐酸后会产生二氧化碳气体;碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳;
【事件反思】在化合物中,氧元素显-2价,则二氧化硅中硅元素显+4价.
故答案为:【探究一】CaO+H2O=Ca(OH)2;
【探究二】放热;
【探究三】烧杯、玻璃棒、漏斗、铁架台(铁圈)、滤纸;用玻璃棒蘸取待测液体,点在pH试纸上,并与标准比色卡对照,得到pH.
| 变红色 | |
| ②取少量沉淀放在试管中,加入盐酸 | 产生无色无味的气体 |
【事件反思】
| +4 |
| Si |
点评:本题考查了常见物质成分的推断,完成此题,可以依据物质的性质结合有关的实验现象进行.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
氢燃料电池是当前为保护环境各国积极发展的一种新型的能源装置,它的基本原理是以氢气和氧气为原料,通过化学反应直接产生电能,运行时产生的温度一般不超过80℃,反应后产物只有水.以下对氢燃料电池的叙述符合事实的是( )
| A、其能量转换过程是:化学能→热能→电能 |
| B、氢气和氧气的化学能全部转化为电能 |
| C、氢燃料电池汽车的使用可以有效减少城市空气污染 |
| D、用水电解制取氢气既经济又方便 |
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数为118,中子数为175的超重元素,该元素原子核内的中子数与核外电子数之差是( )
| A、57 | B、47 | C、61 | D、293 |
下列过程中主要只涉及物理变化的是( )
| A、浓硫酸使白纸变黑 |
| B、氧气供给呼吸 |
| C、生石灰遇水变成熟石灰 |
| D、用酒精浸泡紫罗兰花自制酸碱指示剂 |
火箭主要燃料是偏二甲肼(化学式为C2H8N2).下列有关偏二甲肼的叙述正确的是( )
| A、偏二甲肼是由2个碳原子、4个氢原子、1个氮气分子组成 |
| B、偏二甲肼是由碳、氢、氮三种元素组成 |
| C、偏二甲肼是由2个碳原子、8个氢原子、2个氮气分子组成 |
| D、偏二甲肼中碳、氢、氮 的质量1:4:1 |


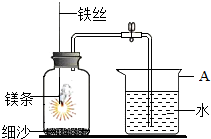 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%.