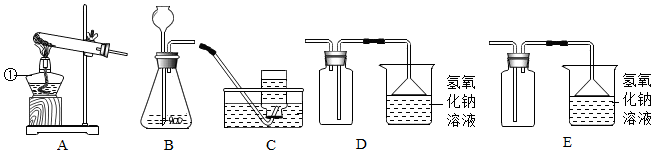
题目内容
19.某同学发现,上个月做实验用的NaOH溶液忘记了盖瓶盖.对于该溶液是否变质,同学们开始实验探究.【猜想假设】
猜想(1):该溶液没有变质,该溶液的溶质为NaOH.
猜想(2):该溶液全部变质,该溶液的溶质为Na2CO3.
猜想(3):该溶液部分变质,该溶液的溶质为NaOH和Na2CO3的混合溶液.
【查阅资料】Na2CO3溶液呈碱性
【设计方案】请你完善下表几组同学探讨的设计方案
| 实验操作 | 可能出现的现象与结论 | 同学评价 | |
| 第1组 | 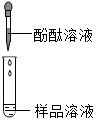 | 若溶液变红,则猜想(2)不成立 | 第2组同学认为:此方案结论不正确,理由是:Na2CO3溶液呈碱性. |
| 第2组 | 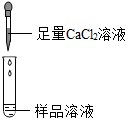 | 若产生白色沉淀,反应方程式是:CaCl2+Na2CO3=CaCO3↓+2NaCl,则猜想(1)不成立. | 第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立. |
| 第3组 | 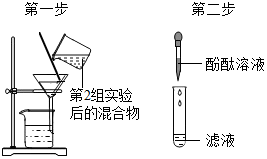 | 若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立. | 第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:直接向变浑浊的溶液中直接滴加酚酞溶液 |
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
分析 根据氢氧化钠能与二氧化碳反应生成碳酸钠和水进行猜想,碳酸钠和氢氧化钠的水溶液都是呈碱性,检验碳酸钠和氢氧化钠的存在,首先需要加入试剂检验并除去碳酸钠,然后加入酚酞试液检验氢氧化钠的存在,据此解答.
解答 解:【猜想假设】若是氢氧化钠没变质,则全部是氢氧化钠,若是氢氧化钠全部变质,则全部是碳酸钠,故填:NaOH;Na2CO3;
第1组:滴加酚酞变红,则不能确定一定是氢氧化钠,因为碳酸钠的水溶液也是呈碱性,也能使酚酞试液变红,故填:Na2CO3溶液呈碱性;
第2组:氯化钙能与碳酸钠反应产生白色碳酸钙沉淀和氯化钠,有沉淀产生,说明一定含有碳酸钠,故猜想(1)不成立,故填:CaCl2+Na2CO3=CaCO3↓+2 NaCl;(1);
第3组:不需要过滤,可以直接向浑浊的液体中加入酚酞试液,根据颜色的变化进行判断即可,故填:直接向变浑浊的溶液中直接滴加酚酞溶液;
由于氢氧化钠能与二氧化碳反应,故需要密封保存,故填:密封.
点评 熟练掌握氢氧化钠、碳酸钠的化学性质,知道氢氧化钠的变质的原因并能够选择合适的方法进行检验.记住反应的化学方程式.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.通过下列实验操作和现象得出的结论是错误的为( )
| 实验操作 | 现象 | 结论 | |
| A | 向失去标签的集气瓶中,插入带火星的木条. | 木条复燃 | 说明集气瓶中装的气体是氧气 |
| B | 在硫酸铜溶液中放入擦拭干净的铁丝 | 铁丝表面有红色物质析出 | 铁的活动性比铜活泼 |
| C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
| D | 点燃从导管放出的A气体,在火 焰上方罩一个内壁蘸有澄清石灰水的烧杯 | 烧杯内壁石灰水变浑浊 | A气体一定含有 碳元素和氧元素 |
| A. | A | B. | B | C. | C | D. | D |
7.如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( )


| A. | C、Fe在氧气中燃烧均会产生大量白烟 | |
| B. | Ⅰ、Ⅱ两类反应均体现了氧气的可燃性 | |
| C. | Fe在Ⅰ、Ⅱ两类反应中的产物不相同 | |
| D. | Ⅰ类反应放出热量,Ⅱ类反应吸收热量 |
4.某化学反应的微观示意图如下,下列说法正确的是( )
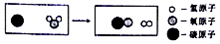

| A. | 生成的两种物质都属于单质 | B. | 生成物的分子个数比为1:1 | ||
| C. | 反应前后元素的化合价不变 | D. | 该反应不属于基本反应类型 |
8.某电视台节目中爆出某品牌金饰品掺假事件,这引起了同学们的好奇心.同学们在老师的帮助下,对鉴别真假黄金进行了相关的探究活动.
【提出问题】怎样鉴别真假黄金?
【查阅资料】假黄金通常是黄铜(Cu-Zn合金)
【实验药品】稀盐酸、硝酸银溶液、硫酸铜溶液、铜丝、银丝
【实验探究】依据所学知识,同学们利用上述药品设计并进行了如下鉴别黄金样品真伪的实验:
【反思总结】
将黄金样品放在空气中高温煅烧能(填“能”或“不能”)鉴别真假黄金.
【知识迁移】
某同学对【实验探究】中的实验方案进行了仔细分析.他认为在以上两组实验方案的基础上要得出铜、银、金的活动性顺序,还需补做一组现象明显的实验是(用化学反应方程式表示)Cu+2AgNO3=2Ag+Cu(NO3)2.
【提出问题】怎样鉴别真假黄金?
【查阅资料】假黄金通常是黄铜(Cu-Zn合金)
【实验药品】稀盐酸、硝酸银溶液、硫酸铜溶液、铜丝、银丝
【实验探究】依据所学知识,同学们利用上述药品设计并进行了如下鉴别黄金样品真伪的实验:
| 实验方案 | 实验现象 | 实验结论 |
| 取黄金样品于试管中,滴加稀盐酸 | 黄金样品表面有 气泡产生 | 此样品为假(选填“真”或“假”)黄金 |
| 取另一黄金样品于试管中,滴加硝酸银溶液 | 无明显现象 | 此样品为真黄金. |
将黄金样品放在空气中高温煅烧能(填“能”或“不能”)鉴别真假黄金.
【知识迁移】
某同学对【实验探究】中的实验方案进行了仔细分析.他认为在以上两组实验方案的基础上要得出铜、银、金的活动性顺序,还需补做一组现象明显的实验是(用化学反应方程式表示)Cu+2AgNO3=2Ag+Cu(NO3)2.
 现有A、B、C、D、E、F六种初中化学常见的物质,在常温下A、B为气体单质,C常用作导线的内部材料,C和D含有相同元素,E是一种溶液,溶质是由两种元素组成的化合物,用两圆间的短线“--”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:(以上反应均在初中知识范围内)
现有A、B、C、D、E、F六种初中化学常见的物质,在常温下A、B为气体单质,C常用作导线的内部材料,C和D含有相同元素,E是一种溶液,溶质是由两种元素组成的化合物,用两圆间的短线“--”表示两种物质可以发生化学反应,箭头“→”表示一种物质能转化为另一种物质.请回答下列问题:(以上反应均在初中知识范围内)