题目内容
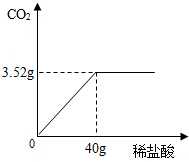 如图为12.5克大理石与稀盐酸溶液反应的关系.计算:
如图为12.5克大理石与稀盐酸溶液反应的关系.计算:(1)大理石中碳酸钙的质量?
(2)40g稀盐酸与大理石恰好完全反应,求稀盐酸中氯化氢(HCl)的质量分数是多少?(保留到0.1%)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据图中数据可以判断生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钙的质量和生成的氯化钙的质量;
(2)根据二氧化碳的质量可以计算稀盐酸中氯化氢(HCl)的质量,进一步可以计算稀盐酸中氯化氢(HCl)的质量分数.
(2)根据二氧化碳的质量可以计算稀盐酸中氯化氢(HCl)的质量,进一步可以计算稀盐酸中氯化氢(HCl)的质量分数.
解答:解:根据图中数据可以判断生成二氧化碳的质量为3.52g
设碳酸钙的质量为x,氯化氢(HCl)的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 3.52g
=
=
x=8g y=5.84g
稀盐酸中氯化氢(HCl)的质量分数是
×100%=14.6%
答案:
(1)大理石中碳酸钙的质量8g
(2)稀盐酸中氯化氢(HCl)的质量分数是14.6%
设碳酸钙的质量为x,氯化氢(HCl)的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 44
x y 3.52g
| 100 |
| x |
| 73 |
| y |
| 44 |
| 3.52g |
x=8g y=5.84g
稀盐酸中氯化氢(HCl)的质量分数是
| 5.84g |
| 40g |
答案:
(1)大理石中碳酸钙的质量8g
(2)稀盐酸中氯化氢(HCl)的质量分数是14.6%
点评:解读折线是初中化学计算中的一种常规题型,解题时首先明确发生的化学反应,再看曲线的三点:起点、折点和终点,获得并处理信息,找到解题突破口,解答试题.

练习册系列答案
相关题目
用分子的观点解释下列事实,其中不正确的是( )
| A、百花盛开,花香四溢--分子在不断的运动 |
| B、50mL水和50mL酒精混合,液体总体积小于100mL--分子之间有间隔 |
| C、湿衣服在阳光下容易干,说明分子的运动速率随温度升高而增大 |
| D、热胀冷缩,说明分子的大小随温度的升高和降低而改变 |
下列物质发生的变化中,属于化学变化的是( )
| A、冰激凌融化 | B、苹果腐烂 |
| C、玻璃打碎 | D、海水晒盐 |
在反应CH4+2O2
CO2+2H2O中,说法错误的是( )
| ||
| A、反应中各物质的质量比是1﹕2﹕1﹕2 |
| B、反应中CH4和O2分子个数比为1﹕2 |
| C、反应符合质量守恒定律 |
| D、反应前后分子数目没变 |

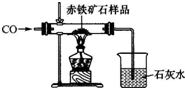 (1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是
(1)小强为了探究某炼铁厂赤铁矿石中氧化铁的质量分数,设计了如图所示的装置进行实验,测出赤铁矿中氧化铁的质量分数为80%.现炼铁厂利用该赤铁矿石5000t,理论上可炼出含铁98%的生铁的质量是