题目内容
2.下列实验现象描述正确的是( )| A. | 硫酸铵和熟石灰固体混合研磨,有刺激性气味气体产生 | |
| B. | 铜丝插入硫酸铝溶液中,溶液由无色变为蓝色 | |
| C. | 点燃棉线,会闻到烧焦羽毛的气味 | |
| D. | 硫在氧气中燃烧,发出蓝紫色火焰,放出热量 |
分析 A、铵态氮肥与碱性物质混合后能放出有刺激性气味的氨气,进行分析判断.
B、根据金属的化学性质进行分析判断.
C、根据棉线燃烧的现象进行分析判断.
D、根据硫在氧气中燃烧的现象进行分析判断.
解答 解:A、硫酸铵属于铵态氮肥,熟石灰具有碱性,混合研磨,有刺激性气味气体产生,故选项说法正确.
B、铜的金属活动性比铝弱,铜丝插入硫酸铝溶液中,不反应而无明显变化,故选项说法错误.
C、点燃棉线,有烧纸的气味,故选项说法错误.
D、硫在氧气中燃烧,发出蓝紫色火焰,放出热量,故选项说法正确.
故选:AD.
点评 本题难度不大,掌握铵态氮肥的性质、金属的化学性质、常见物质燃烧的现象是正确解答本题的关键.

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
13.下列物质在氧气中燃烧,生成物是黑色固体的是( )
| A. | 木炭 | B. | 铁丝 | C. | 镁条 | D. | 红磷 |
10.下列实验中,可验证物质的化学性质的是( )
| A. |  金属刻划 | B. |  闻气味 | C. |  石墨导电 | D. |  鲜花变色 |
17.做铁丝在氧气中燃烧的实验时,要先点燃铁丝上系着的火柴,再伸入集满氧气的集气瓶中,火柴燃烧所起的作用是( )
| A. | 升高铁丝的着火点 | B. | 升高铁丝的温度 | ||
| C. | 增加可燃物 | D. | 增大与氧气的接触面积 |
11.从分子的角度解释“湿衣服晾干”,下列说法错误的是( )
| A. | 水分子在不断运动 | B. | 水分子之间的间隔变大 | ||
| C. | 水分子本身不发生变化 | D. | 水分子的体积变大 |
12.小刘同学想在实验室里用NaOH溶液来制取Na2CO3溶液.
【查阅资料】①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象.
②NaHCO3溶液煮沸时不会发生分解.
③NaHCO3+NaOH=Na2CO3+H2O
④Ca(HCO3)2可溶于水
【制取步骤】①量取两份50mL相同浓度的NaOH溶液备用;
②用一份50mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
③小心煮沸②溶液1-2分钟;
④在得到的③的溶液中加入另一份50mL NaOH溶液,使其充分混合即得.
【实验探究】为了检验制得的溶液是否为纯净的Na2CO3溶液,请你与小刘同学一起完成下列实验探究:
【结论】所制得的溶液为纯净的Na2CO3溶液.
【评价与反思】有人认为实验步骤的顺序对调,即先混合,再煮沸,更合理.你认为对吗?请说明理由:不对,在煮沸之前溶液中含有未参与反应的二氧化碳气体,如果先混合,则氢氧化钠溶液会和溶液中的二氧化碳继续反应,导致制备的碳酸钠不纯净.
【查阅资料】①CO2通入NaOH溶液时极易因CO2过量而产生NaHCO3,且无明显现象.
②NaHCO3溶液煮沸时不会发生分解.
③NaHCO3+NaOH=Na2CO3+H2O
④Ca(HCO3)2可溶于水
【制取步骤】①量取两份50mL相同浓度的NaOH溶液备用;
②用一份50mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
③小心煮沸②溶液1-2分钟;
④在得到的③的溶液中加入另一份50mL NaOH溶液,使其充分混合即得.
【实验探究】为了检验制得的溶液是否为纯净的Na2CO3溶液,请你与小刘同学一起完成下列实验探究:
| 实验步骤 | 实验现象 | 实验结论 | |
| 取少量制得的溶液于试管中,加入过量的CaCl2溶液 | 产生白色沉淀 | 原来制得的溶液中含有Na2CO3 | |
| 将上步实验所得混合物进行过滤,将滤液分成两份 | 取其中一份加入足量的稀盐酸 | 无气泡产生 | 原来制得的溶液中不含碳酸氢钠 |
| 取另一份加入MgCl2溶液 | 无明显现象 | 原来制得的溶液中不含NaOH | |
【评价与反思】有人认为实验步骤的顺序对调,即先混合,再煮沸,更合理.你认为对吗?请说明理由:不对,在煮沸之前溶液中含有未参与反应的二氧化碳气体,如果先混合,则氢氧化钠溶液会和溶液中的二氧化碳继续反应,导致制备的碳酸钠不纯净.
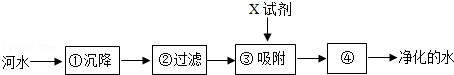
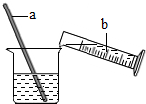 实验室中常需要使用硫酸.
实验室中常需要使用硫酸.