题目内容
某班 同学为验证酸的化学通性,做了五组实验。分析并回答问题。
同学为验证酸的化学通性,做了五组实验。分析并回答问题。

(1)A组试管中都产生H2。若要制得较纯的H2,选稀硫酸而不选盐酸的原因是_____________。
(2)B组试管中实验现象相同,该现象是_______________________________ _。
_。
(3)写 出C组任一试管中发生反应的化学方程式_________________________。
出C组任一试管中发生反应的化学方程式_________________________。
(4)上述五组实验中没有体现酸的通性的是______(填序号)。
【答案】(1)盐酸有挥发性或盐酸会挥发出氯化氢气体或制得的氢气中混有氯化氢气体;(2)红色(或红棕色)固体逐渐减少,溶液变成黄色;(3)NaOH+HCl=NaCl+H2O或2NaOH+H2SO4=Na2SO4+2H2O;(4)D
【解析】
试题分析:(1) A组试管中都产生H2。若要制得较纯的H2,选稀硫酸而不选盐酸的原因是盐酸有挥发性或盐酸会挥发 出氯化氢气体或制得的氢气中混有氯化氢气体;(2) B组试管中实验现象相同,该现象是红色(或红棕色)固体逐渐减少,溶液变成黄色;(3)
出氯化氢气体或制得的氢气中混有氯化氢气体;(2) B组试管中实验现象相同,该现象是红色(或红棕色)固体逐渐减少,溶液变成黄色;(3)  C组任一试管中发生反应的化学方程式NaOH+HCl=NaCl+H2O或2NaOH+H2SO4=Na2SO4+2H2O;(4) 上述五组实验中没有体现酸的通性的是D,因为该组反应不是氢离子表现出来的,而是酸根离子表现出来的性质。
C组任一试管中发生反应的化学方程式NaOH+HCl=NaCl+H2O或2NaOH+H2SO4=Na2SO4+2H2O;(4) 上述五组实验中没有体现酸的通性的是D,因为该组反应不是氢离子表现出来的,而是酸根离子表现出来的性质。
考点:复分解反应的应用

练习册系列答案
相关题目
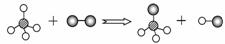
 CuCl2 B. K2CO3
CuCl2 B. K2CO3 KOH
KOH Na2CO3 D. Cu(OH)2
Na2CO3 D. Cu(OH)2 NaOH
NaOH
