题目内容
19.如图是X、Y、Z、W四种溶液的近似pH.下列判断不正确的是( )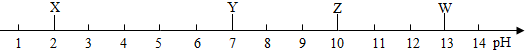
| A. | X一定能使石蕊溶液变红 | B. | Y一定是水 | ||
| C. | Z一定能使酚酞溶液变红 | D. | W的碱性一定比Z强 |
分析 依据pH的应用范围在0~14之间,当pH=7时水呈中性;pH<7时水呈酸性,pH愈小,酸性愈强;当pH>7时水呈碱性,pH愈大,碱性愈强据此分析即可.
解答 解:A、X的pH小于7,显酸性,能使石蕊变红色,故正确;
B、y的pH为7,所以呈中性,但呈中性的溶液不一定是水,如氯化钠的溶液也是中性的,故错误;
C、z的pH为10,大于7,呈碱性,因此z可使无色酚酞溶液变红,故正确;
D、Z的pH为10,W的pH为13,因pH>7时水呈碱性,pH愈大,碱性愈强,故W的碱性一定比Z强,故正确;
故选B.
点评 此题是对溶液pH与酸碱性问题的考查,解题的关键是知道pH的变化规律结合自身的识图分析能力,属常规基础知识考查题

练习册系列答案
相关题目
14.有关反应2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C下列说法不正确的是( )
| A. | 基本反应类型是置换反应 | |
| B. | Mg不能取代红磷测定空气中O2的含量 | |
| C. | CO2发生了氧化反应 | |
| D. | 燃烧可以不需要氧气 |
4.下列两种物质相互混合后,不会发生反应的是( )
| A. | 碳酸钠溶液和氯化钡溶液 | B. | 氢氧化钠溶液和硝酸钡溶液 | ||
| C. | 氢氧化钙溶液和氯化铁溶液 | D. | 盐酸和硝酸银溶液 |
8.酸、碱、盐的溶解性表是学习化学的重要工具,请完成:
(1)碳酸钠和碳酸钾的化学性质相似,是因为其溶液中都含有CO32-(填符号);检验方法和现象是:将样品与足量的盐酸反应,使生成的气体进入澄清的石灰水中,若出现浑浊现象,该样品中含有碳酸根离子;
(2)从表中选择离子组成两种化合物,按要求写化学方程式:
①一个同时有沉淀和气体生成的复分解反应BaCO3+H2SO4=BaSO4↓+H2O+CO2↑;
②一个碱与盐的反应Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
| 离子 | OH- | Cl- | CO3- | SO42- |
| H+ | -- | 溶 | 溶 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 微 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
(2)从表中选择离子组成两种化合物,按要求写化学方程式:
①一个同时有沉淀和气体生成的复分解反应BaCO3+H2SO4=BaSO4↓+H2O+CO2↑;
②一个碱与盐的反应Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
9.通过下列实验操作和现象能得出相应结论的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中,加入约$\frac{1}{3}$瓶体积的NaCl溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2能与NaCl反应 |
| B | 50℃时,将19g KCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时,KCl的溶解度为38g |
| C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |
| A. | A | B. | B | C. | C | D. | D |

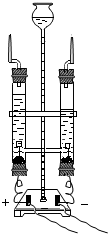 据央视《新闻直播间》2014年12月25日报道,南京鼓楼区一居民家中的自来水检出了两种抗生素的消息,让国人再次聚焦“水安全”.请回答有关问题:
据央视《新闻直播间》2014年12月25日报道,南京鼓楼区一居民家中的自来水检出了两种抗生素的消息,让国人再次聚焦“水安全”.请回答有关问题: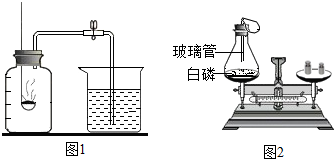 上册化学教材已经两次运用了红磷的燃烧进行实验探究,其所用装置如图所示,请按要求回答下列问题:
上册化学教材已经两次运用了红磷的燃烧进行实验探究,其所用装置如图所示,请按要求回答下列问题: