题目内容
16.某无色溶液由CaCl2、BaCl2、NaCl和Na2CO3四种化合物中的两种组成.向此溶液中加入稀硫酸,生成一种气体.则此溶液中溶质的组成为( )| A. | BaCl2和Na2CO3 | B. | CaCl2和Na2CO3 | C. | BaCl2和NaCl | D. | NaCl和Na2CO3 |
分析 根据碳酸盐与稀硫酸反应能生成使澄清石灰水变浑浊的二氧化碳气体,碳酸盐溶液与钙盐溶液或钡盐溶液反应能生成白色沉淀,稀硫酸和钡离子会生成硫酸钡沉淀等知识进行分析.
解答 解:由于向该溶液中加入稀硫酸时,能生成无色气体,说明该溶液中一定含有碳酸钠,
由于碳酸钠与氯化钙或氯化钡能生成白色沉淀,而该溶液是无色溶液,说明该溶液中一定没有氯化钙和氯化钡;该溶液又是由四种物质中的两种溶于水而成,因此该溶液中除了含有碳酸钠外,一定还含有氯化钠.
故选:D.
点评 本题主要考查碳酸钠、氯化钙、氯化钡和氯化钠的性质,难度稍大.

练习册系列答案
相关题目
7.豆腐鱼菠菜同吃会产生草酸钙,可能影响人体健康,草酸钙的化学式为CaC2O4,草酸钙中碳元素的化合价是( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
4.分别将下列各组物质,同时加到水中,能得到无色透明溶液的是( )
| A. | FeCl3、KOH、NaCl | B. | K2SO4、BaCl2、HCl | ||
| C. | CuSO4、HCl、KCl | D. | Na2CO3、KCl、Na2SO4 |
11.下列说法正确的是( )
| A. | 氢氧化钠和消石灰露置于空气中都会变质 | |
| B. | 铁和铜都可以与稀硫酸反应生成氢气 | |
| C. | 浓盐酸和浓硫酸都可以作气体干燥剂 | |
| D. | 酒精和水只可以作溶剂,不能作溶质 |
1.下列说法不正确的是( )
| A. | 碱分子里氢氧根的数目与金属离子在该碱中的化合价数相等 | |
| B. | 能电离出氢氧根离子的化合物一定是碱 | |
| C. | 由金属离子和酸根离子组成的化合物叫做盐 | |
| D. | KHSO4能电离出H+,但它不是酸,而是盐 |
5.如图是工业上制备氢气的微观示意图,其中不同的“球”代表不同的原子.下列说法不正确的是( )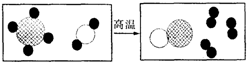

| A. | 工业上制氢气和实验室制氢气反应原理不同 | |
| B. | 反应后的产物必须进行进一步分离才能得到较纯净的氢气 | |
| C. | 该反应属于复分解反应 | |
| D. | 该反应中参加反应的两种分子的个数比为1:1 |
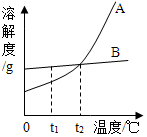 A、B两种固体物质的溶解度曲线如图所示.
A、B两种固体物质的溶解度曲线如图所示.