题目内容
将6.8 g含杂质的锌粒,加入到盛有100g稀硫酸中(杂质不溶于水也不与稀硫酸
反应),充分反应后,称得烧杯内物质的总质量为106.6g。试计算:
(1)生成的氢气质量。
(2)锌粒中所含锌的质量分数(精确到0.1﹪)。
(1)0.2克 (2)95.6%
【解析】
试题分析:(1)根据质量守恒定律可知,产生氢气的质量=6.8 g+100g-106.6g=0.2克,(2)根据氢气质量,利用化学方程式进行计算,得出纯锌的质量,最后用纯锌的质量除以含杂质锌粒质量即可。
【解析】
设 锌粒中所含锌的质量为X
根据质量守恒定律可知,产生氢气的质量=6.8 g+100g-106.6g=0.2克
Zn + H2SO4 ==ZnSO4 + H2↑
2
X 0.2克
65/2=X/0.2克 X=6.5克
所以锌粒中所含锌的质量分数=6.5克/6.8克*100%=95.6%
答:略
考点:利用化学方程式进行含有一定量杂质的计算。

练习册系列答案
相关题目
下图中容器I、II体积相同,起始时红墨水左右两端液面保持相平,若利用针筒将一定量液体同时注入容器中,并迅速关闭弹簧夹,实验过程中有可能观察到红墨水左低右高的是
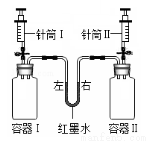
选 项 | 容器I内 | 针筒I内 | 容器II内 | 针筒II内 |
A | 硝酸铵 | 5mL水 | 氢氧化钠 | 5mL水 |
B | 氯化钠 | 5mL水 | 氧化钙 | 5mL水 |
C | 充满二氧化碳 | 5mL氢氧化钠浓溶液 | 充满二氧化碳 | 5mL澄清石灰水 |
D | 0.5g锌粉 | 5g9.8%的稀硫酸 | 0.5g铁粉 | 5g9.8%的稀硫酸 |