题目内容
12.阅读下面科普短文.氮氧化物(NOx)种类很多,造成大气污染的主要是一氧化氮(NO)和二氧化氮(NO2).
NO通常为无色气体.熔点为-163.6℃,沸点为-151.5℃.它的性质不稳定,在空气中易氧化成NO2.NO结合血红蛋白的能力比CO还强,更容易造成人体缺氧.NO分子作为一种传递神经信息的信使分子,在使血管扩张、增强免疫力、记忆力等方面有着极其重要的作用.
NO2通常为红棕色有刺激性气味的气体,溶于水生成硝酸(HNO3)和NO,工业上利用这一原理制取HNO3.NO2能使多种织物褪色,损坏多种织物和尼龙制品,对金属和非金属材料也有腐蚀作用.
城市大气中的NOx大多来自于化石燃料的燃烧.经测算,天然气、煤和石油燃烧产生NOx的量分别为:6.35kg/t、8~9kg/t、9.1~12.3kg/t.以汽油、柴油为燃料的汽车,尾气中NOx的浓度相当高.在非采暖期,北京市一半以上的NOx来自机动车排放.
依据文章内容,回答下列问题:(各答1条即可)
(1)分别说明NO的“利与弊”:“利”是增强记忆力,“弊”是造成大气污染.
(2)与煤和石油相比,天然气是比较清洁的燃料,结合数据解释原因:相同质量时,天然气燃烧产生的NOx的质量少.
(3)减少NOx污染的有效措施绿色出行.
分析 (1)根据NO的“利与弊”进行分析;
(2)根据天然气、煤和石油燃烧产生NOx的量进行分析;
(3)减少NOx污染的根本措施是减少排放.
解答 解:(1)NO分子作为一种传递神经信息的信使分子,在使血管扩张、增强免疫力、记忆力等方面有着极其重要的作用,造成大气污染的主要是一氧化氮(NO)和二氧化氮NO2,城市大气中的NOx大多来自于化石燃料的燃烧.经测算,天然气、煤和石油燃烧产生NOx的量分别为:6.35kg/t、8~9kg/t、9.1~12.3kg/t.以汽油、柴油为燃料的汽车,尾气中NOx的浓度相当高.在非采暖期,NOx主要来自机动车排放;
故答案为:增强记忆力;造成大气污染;
(2)经测算,天然气、煤和石油燃烧产生NOx的量分别为:6.35kg/t、8~9kg/t、9.1~12.3kg/t,从有关数据可以看出,相同质量时,天然气燃烧产生的NOx的质量少,对环境污染小,相对于煤和石油来说是一种比较清洁的能源.
故答案为:相同质量时,天然气燃烧产生的NOx的质量少;
(3)以汽油、柴油为燃料的汽车,所排放的尾气会对空气造污染,减少NOx污染的有效措施是绿色出行.
故答案为:绿色出行.
点评 能源与环保问题是人们关注的热点,也是化学考查的热点,了解常见的能源、常用能源对环境的影响等即可正确解答本题.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
2.实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,某兴趣小组的同学对该样品的成分及含量进行了探究.

【实验探究1】
(1)为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
【实验探究2】为了测定样品中Na2CO3的质量分数,亮亮同学设计如图装置(铁架台略去)按下列步骤进行实验.
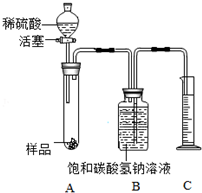
①按图连接好装置并检查装置气密性;
②用托盘天平准确称取6g该样品,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;
③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞;反应结束后,量筒中收集到溶液110mL.
(2)写出A中发生反应的一个化学方程式为2NaOH+H2SO4=Na2SO4+2H2O.
(3)实验中取用样品的质量不宜过多,如果样品用量过多,造成的后果是样品过多,中和反应放热太多使得气体膨胀,测量误差偏大;
(4)已知在实验条件下,二氧化碳的密度为2g•L-1,则生成CO2的质量为0.22g,样品中碳酸钠的质量分数为88.3%.
(5)实验过程中,操作正确,装置气密性良好,Na2CO3质量分数仍将偏大(填“偏大”或“偏小”),理由是加入硫酸溶液的体积也将计入二氧化碳的体积,造成碳酸钠偏多,所以碳酸钠的质量分数偏大.
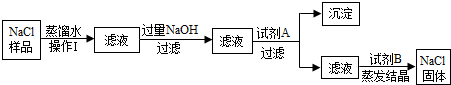
【实验探究3】为了得到较纯净的氢氧化钠固体,杨明同学设计了如图所示的实验流程.
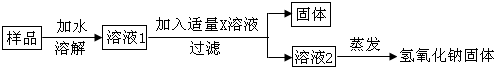
(6)加入适量X溶液是Ca(OH)2溶液.
(7)最终所得氢氧化钠固体的质量大于变质样品中氢氧化钠的质量(选填“大于”、“等于”或“小于”).

【实验探究1】
(1)为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (a)取少量样品于试管中,加水溶解后,加入过量的氯化钙溶液; | 有白色沉淀产生 | 样品中含有碳酸钠 |
| (b)静置,取上层清液于试管中,滴加酚酞试液. | 溶液变红色 | 样品中含有氢氧化钠 |

①按图连接好装置并检查装置气密性;
②用托盘天平准确称取6g该样品,放入A中试管内,向B中集气瓶中倒入饱和碳酸氢钠溶液至瓶颈处;
③向分液漏斗中加入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞;反应结束后,量筒中收集到溶液110mL.
(2)写出A中发生反应的一个化学方程式为2NaOH+H2SO4=Na2SO4+2H2O.
(3)实验中取用样品的质量不宜过多,如果样品用量过多,造成的后果是样品过多,中和反应放热太多使得气体膨胀,测量误差偏大;
(4)已知在实验条件下,二氧化碳的密度为2g•L-1,则生成CO2的质量为0.22g,样品中碳酸钠的质量分数为88.3%.
(5)实验过程中,操作正确,装置气密性良好,Na2CO3质量分数仍将偏大(填“偏大”或“偏小”),理由是加入硫酸溶液的体积也将计入二氧化碳的体积,造成碳酸钠偏多,所以碳酸钠的质量分数偏大.
【实验探究3】为了得到较纯净的氢氧化钠固体,杨明同学设计了如图所示的实验流程.

(6)加入适量X溶液是Ca(OH)2溶液.
(7)最终所得氢氧化钠固体的质量大于变质样品中氢氧化钠的质量(选填“大于”、“等于”或“小于”).
7.某同学在家不慎被蜜蜂蜇伤,蜜蜂的刺液呈酸性,为了减轻痛痒,在蜇伤处涂抹的物质是( )
| A. | 牛奶(pH≈6) | B. | 苹果汁(pH≈3) | C. | 牙膏(pH≈9) | D. | 矿泉水(pH≈7) |
1.下列家庭小实验中不发生化学变化的是( )
| A. | 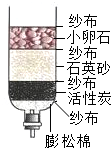 自制简易净水器 | B. |  推测鸡蛋壳成分 | ||
| C. |  自制“叶脉书签” | D. | 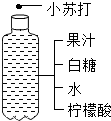 自制汽水 |
2.正确、规范的实验操作是科学探究成败的关键因素之一.下列实验操作不正确的是( )
| A. | 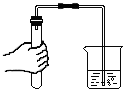 检查气密性 | B. | 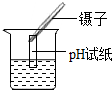 测定溶液pH | C. | 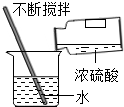 稀释浓硫酸 | D. | 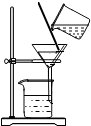 过滤 |
 水是一切生物生存所必需的,我们应该了解有关水的一些知识.
水是一切生物生存所必需的,我们应该了解有关水的一些知识.