题目内容
8.如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题: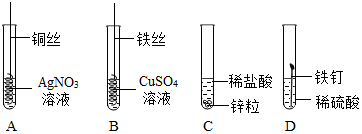
(1)描述B中的实验现象铁丝表面附着了一层红色固体、溶液由蓝色变成浅绿色.
(2)写出A中反应的化学方程式Cu+2AgNO3=Cu(NO3)2+2Ag.
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是AB(填序号).
(4)开始反应后D中无气泡,原因是铁钉表面被氧化.
分析 铜能和硝酸银反应生成硝酸铜和银,铁能和硫酸铜反应生成硫酸亚铁和铜;
铁钉容易被空气中的氧气氧化成铁的氧化物,铁的氧化物和稀硫酸反应生成盐和水.
解答 解:(1)B中的实验现象是:铁丝表面附着了一层红色固体,溶液由蓝色变成浅绿色.
故填:铁丝表面附着了一层红色固体;溶液由蓝色变成浅绿色.
(2)A中铜和硝酸银反应生成硝酸铜和银,反应的化学方程式为:Cu+2AgNO3=Cu(NO3)2+2Ag.
故填:Cu+2AgNO3=Cu(NO3)2+2Ag.
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是AB,通过A可知铜比银活泼,通过B可知铁比铜活泼.
故填:AB.
(4)开始反应后D中无气泡,原因是铁钉表面被氧化,稀硫酸消耗铁钉表面的氧化物反应生成盐和水,当氧化物完全反应后,铁再和稀硫酸反应生成硫酸亚铁和氢气.
故填:铁钉表面被氧化.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
2.化学是一门以实验为基础的自然学科.下列是初中化学课堂演示实验或学生分组实验的部分实验图示,请根据实验图示说出实验目的、现象、结论、物质的性质和作用、化学反应的方程式:
(1)实验①中,用于测定空气中氧气的含量,实验所用的物质是磷(木炭、磷、铁丝).
(2)实验②中,预先在集气瓶里装有少量的水,其目的是防止生成物熔化溅落下来炸裂集气瓶.
(3)实验③中,制取气体的化学反应方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;收集气体用向上排空气法,说明制取气体的密度比空气的密度大(填“大”或“小”或“相同”);证明集气瓶里已收集满气体的实验操作方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)实验④中,将溶液进行过滤得操作时,玻璃棒在实验过程中所起的作用是引流.
(5)实验⑤中,观察到烧杯A中溶液逐渐变成红色,该实验的结论是分子在不断运动.
(6)实验⑥中,根据水中白磷没有燃烧的原理,举出生活中一灭火的事例如用灯帽盖灭酒精灯.
(7)实验⑦中,向烧杯里燃着阶梯蜡烛倾倒CO2气体,观察到的现象是下面的蜡烛先熄灭,然后上面的蜡烛才熄灭.
(8)实验⑧中,用于除去CO中少量的CO2,溶液里发生的化学反应方程式是CO2+2NaOH=Na2CO3+H2O.
| 实验编号 | 实验① | 实验② | 实验③ | 实验④ |
| 实验图示 |  |  | 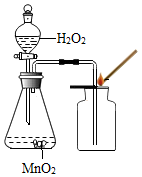 |  |
| 实验编号 | 实验⑤ | 实验⑥ | 实验⑦ | 实验⑧ |
| 实验图示 |  |  |  |  |
(2)实验②中,预先在集气瓶里装有少量的水,其目的是防止生成物熔化溅落下来炸裂集气瓶.
(3)实验③中,制取气体的化学反应方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;收集气体用向上排空气法,说明制取气体的密度比空气的密度大(填“大”或“小”或“相同”);证明集气瓶里已收集满气体的实验操作方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)实验④中,将溶液进行过滤得操作时,玻璃棒在实验过程中所起的作用是引流.
(5)实验⑤中,观察到烧杯A中溶液逐渐变成红色,该实验的结论是分子在不断运动.
(6)实验⑥中,根据水中白磷没有燃烧的原理,举出生活中一灭火的事例如用灯帽盖灭酒精灯.
(7)实验⑦中,向烧杯里燃着阶梯蜡烛倾倒CO2气体,观察到的现象是下面的蜡烛先熄灭,然后上面的蜡烛才熄灭.
(8)实验⑧中,用于除去CO中少量的CO2,溶液里发生的化学反应方程式是CO2+2NaOH=Na2CO3+H2O.
3.下列关于水的说法正确的是( )
| A. | 水结冰发生化学变化 | |
| B. | 水污染都是工业“三废”的任意排放造成的 | |
| C. | 电解水是电能转化成化学能 | |
| D. | 我国水资源丰富,无需节约使用 |
16.下列关于水的说法正确的是( )
| A. | 水能溶解所有物质 | |
| B. | 生活中常用肥皂水检验软水和硬水 | |
| C. | 长期饮用蒸馏水有利于身体健康 | |
| D. | 经过沉淀,过滤后得到的矿泉水是纯净物 |
18.电子工业制作电路板的过程中,用FeCl3溶液来溶解电路板中多余的铜,反应如下:2FeCl3+Cu═2FeCl2+CuCl2.FeCl3溶液也可跟铁发生反应:2FeCl3+Fe═3FeCl2.现向FeCl3溶液中加入一定量的铁粉和铜粉,充分反应后,发现有固体剩余.下面有关说法正确的是( )
| A. | 向剩余的固体加入稀盐酸,若无气体放出,说明反应后的溶液中没有Cu2+ | |
| B. | 若剩余固体是铜与铁的混合物,则说明两种金属都有部分溶解 | |
| C. | 剩余固体只含有铜 | |
| D. | 剩余固体中如果有铁,一定也有铜 |
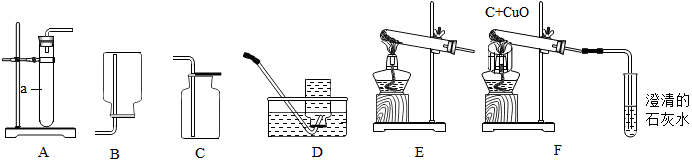
 如图是我们所熟悉的实验室制取气体的常见装置,请回答有关问题:
如图是我们所熟悉的实验室制取气体的常见装置,请回答有关问题: