题目内容
8.如图所示,是为了验证稀硫酸化学性质所做的三个实验,回答下列问题.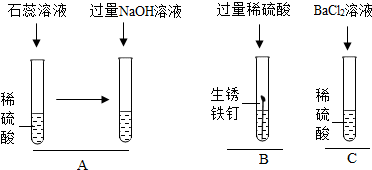
(1)A实验最终能观察到的现象是溶液变蓝;
(2)B实验能体现出稀硫酸具有的化学性质是能与金属氧化物和金属反应;
(3)C实验中发生反应的化学方程式为H2SO4+BaCl2═BaSO4↓+2HCl;
(4)将上述实验后所得溶液在烧杯中混合,观察到烧杯底部有沉淀,上层为有色溶液,此时,利用烧杯中的沉淀,再选择适当的试剂,即可证明C实验中所加BaCl2溶液过量,实验的操作及现象是取AB实验后的溶液与C混合,若沉淀的质量增加,则证明实验中所加BaCl2溶液过量取烧杯底部的沉淀适量于试管中加入过量的稀盐酸或稀硝酸,若沉淀不消失或沉淀部分消失,证明C中所加氯化钡溶液是过量的;若沉淀全部消失,证明氯化钡是不过量的.
分析 (1)根据指示剂的变色情况分析;
(2)根据酸的通性分析;
(3)氯化钡与硫酸反应生成硫酸钡沉淀和氯化氢;
(4)取烧杯底部的沉淀适量于试管中加入过量的稀盐酸或稀硝酸,若沉淀不消失或沉淀部分消失,证明C中所加氯化钡溶液是过量的;若沉淀全部消失,证明氯化钡是不过量的.
解答 解:(1)氢氧化钠过量,溶液呈碱性,石蕊显蓝色;
(2)铁锈的主要成分是氧化铁,是金属氧化物,与硫酸反应生成硫酸铁和水,被硫酸反应完后,里面的铁继续与硫酸反应生成硫酸亚铁和氢气;
(3)氯化钡与硫酸反应生成硫酸钡沉淀和氯化氢,化学方程式为:H2SO4+BaCl2═BaSO4↓+2HCl;
(4)取烧杯底部的沉淀适量于试管中加入过量的稀盐酸或稀硝酸,若沉淀不消失或沉淀部分消失,证明C中所加氯化钡溶液是过量的;若沉淀全部消失,证明氯化钡是不过量的.
故答案为:(1)溶液变蓝;
(2)能与金属氧化物和活泼金属反应;
(3)H2SO4+BaCl2═BaSO4↓+2HCl;
(4)取烧杯底部的沉淀适量于试管中加入过量的稀盐酸或稀硝酸,若沉淀不消失或沉淀部分消失,证明C中所加氯化钡溶液是过量的;若沉淀全部消失,证明氯化钡是不过量的.
点评 掌握酸的化学性质是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列化学用语书写无误的是( )
| A. | 氖的元索符号:Na | B. | 3个氢分子:3H2 | ||
| C. | 2个氧原子:02 | D. | 铝元索显+3价:Al3+ |
16.下列说法中,错误的是( )
| A. | 氢气、石油都是储量丰富的清洁能源 | |
| B. | 滥用化肥、农药会造成水体污染 | |
| C. | 油脂、糖类都是人体所需的营养物质 | |
| D. | 用灼烧法可区分羊毛和合成纤维 |
5.某校研究性学习小组在做与催化剂有关的课题,开展了以下探究,请你参与:
【探究一】验证二氧化锰能加快过氧化氢的分解
(1)请在下表的空白处填写相应的内容
(2)小组一部分同学依据实验①和②现象,就得出结论:二氧化锰能加快过氧化氢的分解.志强同学提出质疑:过氧化氢溶液中含有水,需增加一个对比实验,结论才更严谨,请你帮他设计实验操作:
(3)请写出实验②的反应化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
【探究二】探究氧化铁是否像二氧化锰一样可作氯酸钾分解的催化剂
同学们设计了三组实验(其他可能影响因素均控制相同):
(4)若T3<(选填“>”、“=”或“<”)T1,说明氧化铁能加快氯酸钾的分解.
(5)若要充分证明氧化铁是氯酸钾分解的催化剂,在确认了氧化铁能加快氯酸钾的分解后,还要验证它在化学反应前后的质量和化学性质不变.请你设计实验验证其中一种“不变”:如将实验⑥充分反应后的固体进行溶解、过滤、洗涤、干燥后称量,质量为0.5g,说明氧化铁在反应前后质量不变.
(6)若要比较氧化铁与二氧化锰对氯酸钾分解的催化效果,除了可以通过用比较T3与T2的大小,还可以通过排水法收集氧气,测量相同时间产生氧气体积的大小进行比较,得出结论.
【探究一】验证二氧化锰能加快过氧化氢的分解
(1)请在下表的空白处填写相应的内容
| 实验编号 | 实验操作 | 实验现象 |
实验① | 取10mL5%的过氧化氢溶液于试管中,过一会儿把带火星的木条伸入试管中 | 有少量气泡产生,木条不复燃 |
实验② | 取10mL5%的过氧化氢溶液于试管中,加入少量二氧化锰,把带火星的木条伸入试管中 | 有大量气泡产生,木条复燃 |
| 实验编号 | 实验操作 | 实验现象 |
实验③ | 取10mL蒸馏水于试管中,加入少量二氧化锰,把带火星的木条伸入试管中 | 无气泡产生,木条不复燃 |
【探究二】探究氧化铁是否像二氧化锰一样可作氯酸钾分解的催化剂
同学们设计了三组实验(其他可能影响因素均控制相同):
| 实验编号 | 实验药品 | 分解温度(℃) |
| 实验④ | 1.2gKClO3 | T1 |
| 实验⑤ | 1.2gKClO3、0.5gMnO2 | T2 |
| 实验⑥ | 1.2gKClO3、0.5gFe2O3 | T3 |
(5)若要充分证明氧化铁是氯酸钾分解的催化剂,在确认了氧化铁能加快氯酸钾的分解后,还要验证它在化学反应前后的质量和化学性质不变.请你设计实验验证其中一种“不变”:如将实验⑥充分反应后的固体进行溶解、过滤、洗涤、干燥后称量,质量为0.5g,说明氧化铁在反应前后质量不变.
(6)若要比较氧化铁与二氧化锰对氯酸钾分解的催化效果,除了可以通过用比较T3与T2的大小,还可以通过排水法收集氧气,测量相同时间产生氧气体积的大小进行比较,得出结论.
12.如图所示图象能正确反映对应变化关系的是( )
| A. | 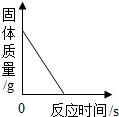 加热一定量高锰酸钾固体制取氧气 | |
| B. | 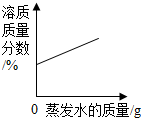 在恒温的条件下,将足量的氯化钠饱和溶液蒸发适量的水分 | |
| C. | 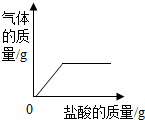 向露置在空气中部分变质的氢氧化钠溶液中逐滴加入稀盐酸 | |
| D. | 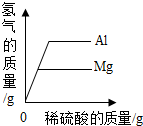 等质量的铝和镁,分别与足量、等溶质质量分数的稀硫酸反应 |
9.对于下列几种化学符号,有关说法正确的是( )
①H ②Fe2+ ③Cu ④P2O5 ⑤Fe3+⑥NaCl.
①H ②Fe2+ ③Cu ④P2O5 ⑤Fe3+⑥NaCl.
| A. | 能表示一个分子的是①④⑥ | |
| B. | ④中的数字“5”表示五氧化二磷中有5个氧原子 | |
| C. | 表示物质组成的化学式是③④⑥ | |
| D. | ②⑤的质子数相同,化学性质也相同 |
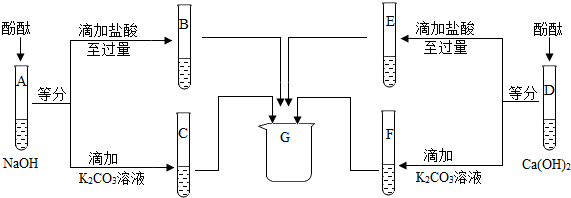
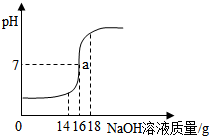 小丽在实验室进行酸碱中和实验,她将未知浓度的NaOH溶液逐滴加入到质量为20g浓度为14.6%的稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.请回答:
小丽在实验室进行酸碱中和实验,她将未知浓度的NaOH溶液逐滴加入到质量为20g浓度为14.6%的稀盐酸中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化如图所示.请回答: