题目内容
10.某同学加热氯酸钾与二氧化锰的混合物16.5g制取氧气,加热过程中测得试管内剩余固体物质的质量随时间变化如表所示:| 反应时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
| 剩余固体物质的质量/g | 15.9 | 14.6 | 12.2 | 11.7 | 11.7 | 11.7 |
(1)该同学制得氧气的质量为多少?
(2)加热到5min时剩余固体中氯化钾的质量为多少?
分析 氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)该同学制得氧气的质量为:16.5g-11.7g-=4.8g,
答:该同学制得氧气的质量为4.8g.
(2)设加热到5min时剩余固体中氯化钾的质量为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
149 96
x 4.8g
$\frac{149}{x}$=$\frac{96}{4.8g}$,
x=7.45g,
答:加热到5min时剩余固体中氯化钾的质量为7.45g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
20.将10g溶质质量分数为20%的氢氧化钠溶液与20g溶质质量分数为10%的硫酸溶液混合后,下列物质中不能与该溶液发生反应的是( )
| A. | CuCl2 | B. | Na2CO3 | C. | CO2 | D. | Ba(NO3)2 |
1.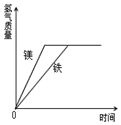 有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.
有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.
下列结果可能的是( )
 有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.
有等质量的镁和铁,镁放入质量分数为10%的稀硫酸中,铁放入质量分数为10%的稀盐酸中,产生氢气的质量随反应时间变化曲线如图所示.下列结果可能的是( )
| ①反应后镁有剩余 | ②反应后铁有剩余 |
| ③反应后稀硫酸有剩余 | ④反应后稀盐酸有剩余 |
| ⑤剩余铁的和镁的质量相等 | ⑥消耗的稀硫酸和稀盐酸质量相等. |
| A. | ①③⑤ | B. | ①②⑥ | C. | ①④ | D. | ②③⑥ |
5.某品牌矿泉水的标签上的内容如表所示,下列说法中,不正确的是( )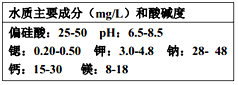

| A. | 该品牌矿泉水为混合物 | |
| B. | 该品牌的矿泉水一定呈酸性 | |
| C. | “锶、钠、钙、镁、钾”属于金属元素 | |
| D. | 饮用该矿泉水可以为人体补充人体所需的无机盐 |
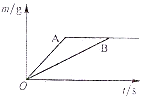 将等质量的锌粉和铁粉分别放入质量相等、浓度相同的稀硫酸中,生成氢气的质量(m)随时间(t)的变化曲线如图,请回答
将等质量的锌粉和铁粉分别放入质量相等、浓度相同的稀硫酸中,生成氢气的质量(m)随时间(t)的变化曲线如图,请回答