题目内容
13.取5g氧化镁与氧化铜的混合物,加入溶质质量分数为9.8%的稀硫酸100g,恰好完全反应生成盐和水.原混合物中氧元素的质量是( )| A. | 6.4g | B. | 3.2g | C. | 1.8g | D. | 1.6g |
分析 根据氧化铜和硫酸反应生成硫酸铜和水,氧化镁和硫酸反应生成硫酸镁和水,再根据氧元素的质量守恒进行分析解答.
解答 解:由于氧化铜和氧化镁的混合物与100克9.8%的稀硫酸恰好完全反应,分析化学方程式可知氧化物中氧元素全部转变为水中的氧元素,计算出水的质量进而计算出所含氧元素的质量即可;
设氧元素的质量是x:由方程式可以看出硫酸与生成水的关系为
H2SO4 ~H2O∽~O
98 18 16
100g×9.8% x
$\frac{98}{100g×9.8%}$=$\frac{16}{x}$
x=1.6g
故选:D.
点评 本题很好的考查了质量守恒定律的应用,解答时首先分析实验的反应原理,再根据反应原理,根据化学方程式计算出该样品中某一成分的质量,得出所要探究的物质中该成分的含量.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
8.实验是化学科学研究的主要手段.下列化学实验操作正确的是( )
| A. | 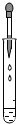 取用少量液体 | B. | 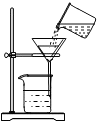 过滤 | C. |  闻气味 | D. | 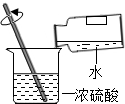 稀释浓硫酸 |
5.现有等质量的铁粉、镁粉、锌粉,在相同温度下分别跟足量的同浓度的稀硫酸反应.他们中产生氢气最快最多的是( )
| A. | 铁粉 | B. | 镁粉 | C. | 锌粉 | D. | 没有差别 |
2.关于催化剂的说法正确的是( )
| A. | 使用催化剂可增加生成物的质量 | |
| B. | 加入催化剂一定能使反应速率加快 | |
| C. | 不使用催化剂反应就不能发生 | |
| D. | 催化剂在反应前后的质量与化学性质都不变 |
3.最近,科学家用一种含钼的化合物作催化剂,在常温下就能完成氨的合成,大大降低了生产成本,使得液氨有望取代液氢成为新一代绿色能源.氨合成反应方程式为:N2+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3,下列说法中错误的是( )
| A. | 上述反应属于化合反应 | |
| B. | NH3中氮元素的化合价为+3价 | |
| C. | NH3中氮元素和氢元素的质量之比是14:3 | |
| D. | 上述反应中的反应物、生成物都是由分子构成的 |