题目内容
金属是一种非常重要的资源,在生产、生活中有着广泛的用途.
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁.用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的化学方程式为 .
(2)每年世界上钢铁的产量很高,可全世界每年因生锈损失的钢铁约占世界钢铁年产量的
,这给人类带来了巨大的损失.铁在空气中锈蚀,实际上是铁跟空气中的 共同作用的结果.现有一批铁质螺丝钉已经开始生锈,你能用化学方法除锈,并做防锈处理吗?请简要写出你的做法及涉及到的化学方程式 .
(3)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请回答下列问题:
①亮亮所用的另一种溶液是 .
②说明Mg比Fe活泼的实验现象是 .
③说明Cu比Ag活泼的实验现象是 .
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁.用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的化学方程式为
(2)每年世界上钢铁的产量很高,可全世界每年因生锈损失的钢铁约占世界钢铁年产量的
| 1 |
| 4 |
(3)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请回答下列问题:
①亮亮所用的另一种溶液是
②说明Mg比Fe活泼的实验现象是
③说明Cu比Ag活泼的实验现象是
考点:铁的冶炼,金属活动性顺序及其应用,金属锈蚀的条件及其防护,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据金属铁的冶炼原理方程式解答;(2)根据铁锈蚀的条件和化学方法除锈措施来分析;(3)金属和酸反应时,只有在金属活动性顺序表中氢前的金属可以置换出酸中的氢离子,而且越靠前的金属反应越剧烈;金属和盐反应时,在金属活动性顺序表中只有前面的金属可以把它后面的金属从盐溶液中置换出来,钾、钙、钠除外.
解答:解:(1)用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的反应物是一氧化碳和氧化铁,写在等号的左边,生成物铁和二氧化碳写在等号的右边,根据得失氧进行配平,反应条件是高温写在等号的上边,所以化学方程式为:3CO+Fe2O3
2Fe+3CO2;
(2)钢铁生锈是铁与空气中的水、氧气共同作用的结果,除锈可以用稀硫酸或稀盐酸;
(3)由于镁和铁都在氢前,都能和稀盐酸反应,而且反应剧烈的是镁,而铜和银都不能和盐酸反应,为证明两金属的金属活动性强弱,可选用硝酸银溶液或硫酸铜溶液.
故答案为:(1)3CO+Fe2O3
2Fe+3CO2;(2)水、氧气;用适量的稀硫酸浸泡至铁锈消失,然后再用水冲洗干净,干燥后涂上些油从而防锈:Fe2O3+H2SO4=Fe2(SO4)3+3H2O;(3)①硝酸银溶液(或硫酸铜溶液);②冒出气泡的速率快;③铜丝表面有一层银白色物质生成.
| ||
(2)钢铁生锈是铁与空气中的水、氧气共同作用的结果,除锈可以用稀硫酸或稀盐酸;
(3)由于镁和铁都在氢前,都能和稀盐酸反应,而且反应剧烈的是镁,而铜和银都不能和盐酸反应,为证明两金属的金属活动性强弱,可选用硝酸银溶液或硫酸铜溶液.
故答案为:(1)3CO+Fe2O3
| ||
点评:该题难度适中,主要考查了对铁的冶炼和金属活动性顺序的灵活运用,培养学生应用知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
乙酸乙酯(C4H8O2) 常用于食品中以增强食物的芳香性.下列关于乙酸乙酯的说法正确的是( )
| A、碳元素的质量分数为36.6% |
| B、摩尔质量为88 |
| C、碳、氢、氧三种元素质量比为2:4:1 |
| D、每个分子由4个碳原子、8个氢原子和2个氧原子构成 |
 右图是某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥的过程,其中试剂甲和乙分别可能是
右图是某同学鉴别NH4HCO3、NH4Cl、KCl三种化肥的过程,其中试剂甲和乙分别可能是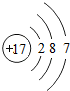 如图是氯元素的原子结构示意图,该原子的核电荷数为
如图是氯元素的原子结构示意图,该原子的核电荷数为