题目内容
6.下列图象能正确反映对应变化关系的是( )| A. | 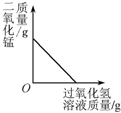 向一定量的二氧化锰中加入过氧化氢溶液 | |
| B. | 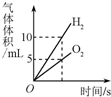 将水通电电解一段时间 | |
| C. | 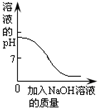 向稀盐酸中加入氢氧化钠溶液 | |
| D. | 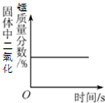 加热一定量的氯酸钾和二氧化锰的混合物 |
分析 A、根据二氧化锰在过氧化氢分解的过程中作催化剂,反应前后质量不变解答;
B、根据电解水时产生的氢气和氧气的体积比是2:1,进行分析判断;
C、根据稀盐酸的pH小于7解答;
D、根据氯酸钾分解产生了氧气,反应后锰元素的质量分数发生了改变解答.
解答 解:
A、二氧化锰在过氧化氢分解的过程中作催化剂,反应前后质量不变,图象应成一条水平直线,故图象与实验操作过程不对应.
B、将水通电电解一段时间,水通电产生氢气和氧气的体积比是2:1,而不是质量比为2:1,故图象与实验操作过程对应.
C、稀盐酸的pH小于7,向稀盐酸中加入氢氧化钠溶液,酸性减弱,pH增大,故图象与实验操作过程不对应.
D、氯酸钾分解产生了氧气,使固体的总质量减少,虽然锰元素的质量不变,但反应前后锰元素的质量分数应增大,完全分解后不变,图象应该是先上升后故选:B.
点评 本题是一道图象坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图象.

练习册系列答案
相关题目
8.当今人类使用的三大化石燃料为( )
| A. | 煤、石油、氢气 | B. | 汽油、柴油、液化石油气 | ||
| C. | 甲烷、天然气、乙醇 | D. | 煤、石油、天然气 |
9.在A+3B═2C+2D的反应中,7gA和24gB恰好完全反应生成C和D,若B和D的相对分子质量之比为16:9,则生成C的质量为( )
| A. | 16g | B. | 22g | C. | 44g | D. | 88g |
11.对分子、原子的认识,正确的是( )
| A. | 原子能构成分子,但不能直接构成物质 | |
| B. | 分子由原子构成,原子不能再分 | |
| C. | 分子是保持物质化学性质的一种微粒 | |
| D. | 固体难压缩,说明固体分子间无间隔 |
18.小明在实验室发现一瓶氢氧化钠固体没有塞上瓶塞,于是他和他的同学一起对这瓶氢氧化钠固体展开探究,请你与他们一起进行探究.【提出问题】这瓶氢氧化钠固体是否变质?
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质.
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
【反思与交流】
(4)久置的氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH=Na2CO3+H2O.
【探索与拓展】(5)为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为115.6g.求该样品中碳酸的质量分数(要写出计算过程).
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质.
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸 | 有气泡产生 | 猜想①不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液 | 产生白色沉淀 | 反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液 | 溶液呈红色 | 猜想②成立 |
(4)久置的氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH=Na2CO3+H2O.
【探索与拓展】(5)为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为115.6g.求该样品中碳酸的质量分数(要写出计算过程).
16.溶液是生产生活中常见的物质,依据相关信息回答问题:
资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如表所示:
(1)农业上,硝酸钾用作水溶性肥料,为作物补充氮和钾元素.硝酸钾溶液中的溶质是硝酸钾(KNO3).
(2)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示.

①(填字母序号)ABC中盛的一定是饱和溶液.
②使B烧杯的溶液升温至50℃时,溶液的质量为186 g.
③采用一种方法使A中的固体恰好溶解.对于最终四个烧杯中的溶液,下列说法正确的是acd(填字母序号).
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(3)工业上利用电解饱和氯化钠溶液可制得重要化工产品氢氧化钠.氢氧化钠溶液可用于治理含二氧化硫的废气并回收二氧化硫,反应的主要流程如下:

①实际生产中,在一定温度下,配制100t溶质的质量分数为25%的饱和氯化钠溶液,需水的质量为75t.
②以上流程中,可循环使用的物质是氯化钠(NaCl).
③亚硫酸氢钠(NaHSO3)中硫元素的质量分数为30.8%(计算结果精确到0.1%).
资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如表所示:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶解度/g | 21 | 32 | 46 | 64 | 86 | 110 | 138 |
(2)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示.

①(填字母序号)ABC中盛的一定是饱和溶液.
②使B烧杯的溶液升温至50℃时,溶液的质量为186 g.
③采用一种方法使A中的固体恰好溶解.对于最终四个烧杯中的溶液,下列说法正确的是acd(填字母序号).
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(3)工业上利用电解饱和氯化钠溶液可制得重要化工产品氢氧化钠.氢氧化钠溶液可用于治理含二氧化硫的废气并回收二氧化硫,反应的主要流程如下:

①实际生产中,在一定温度下,配制100t溶质的质量分数为25%的饱和氯化钠溶液,需水的质量为75t.
②以上流程中,可循环使用的物质是氯化钠(NaCl).
③亚硫酸氢钠(NaHSO3)中硫元素的质量分数为30.8%(计算结果精确到0.1%).