题目内容
18.根据下列装置图回答问题.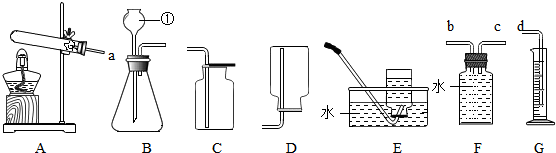
(1)标号仪器①的名称是长颈漏斗.
(2)实验室制取二氧化碳,应选择的发生装置是B(填字母序号,下同),收集装置为C.
(3)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收集到的氧气体积(装置选用A、F、G).
①写出该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
②若各装置的连接顺序是:a→b→c→d,F装置内导管(“b”或“c”)该怎样延伸?请在F中画出来.
③根据高锰酸钾的质量算出的氧气体积为理论值.如果实际测得氧气的体积大于理论值(水的体积测量准确),你认为原因是未冷却到室温就读数.
④若改用氯酸钾和二氧化锰来制取氧气,则二氧化锰在反应前后固体混合物中的质量分数将变大(填“变大”、“变小”或“不变”)
分析 (1)熟记标号仪器的名称;
(2)根据实验室中制取二氧化碳的反应原理和反应条件来选择反应的发生装置,由二氧化碳的密度及水溶性来选择收集装置;
(3)实验室用一定质量的高锰酸钾制取氧气,通过排水量测定所收集到的氧气体积:
①正确书写高锰酸钾制取氧气的化学方程式;
②若各装置的连接顺序是:a→b→c→d,F装置内导管,c管延长,有利于排水;
③了解正确读数的时机,待冷却到室温再读数;
④根据化学方程式:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑可知,二氧化锰在反应前后固体混合物中的质量分数的变化.
解答 解:(1)①是长颈漏斗;故填:长颈漏斗;
(2)在实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,属于固液常温型,所以应该选择B装置来制取二氧化碳气体;二氧化碳密度比空气大,能溶于水,所以应该选择C装置来收集二氧化碳.故填:B;C;
(3)①正确书写高锰酸钾制取氧气的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
②若各装置的连接顺序是:a→b→c→d,F装置内导管,c管延长,有利于排水,故如图 ;
;
③根据高锰酸钾的质量算出的氧气体积为理论值.如果实际测得氧气的体积大于理论值(水的体积测量准确),原因是:未冷却到室温就读数;
④根据化学方程式:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑可知,二氧化锰在反应前后固体混合物中的质量分数的变化为变大.
故答案为:①2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
② ;
;
③未冷却到室温就读数;
④变大.
点评 本题主要考查了实验室根据反应原理和气体的密度和水溶性制取氧气、二氧化碳的装置的选取;了解常用气体的收集方法;根据题目中的信息正确有关书写化学方程式.

| A. | 生石灰 | B. | 浓硫酸 | C. | 硝酸铵 | D. | 烧碱 |
| A. | 釜底抽薪-取出可燃物,使燃烧更旺 | |
| B. | 火上加油-增加易燃物,使火势燃得更加旺盛 | |
| C. | 煽风点火-使空气流通,为燃烧补充空气或氧气 | |
| D. | 钻木取火-摩擦生热,使可燃物的温度达到着火点而燃烧 |
 某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图所示的“吸金球”,“吸金球”是装有一些“吸金”物质的纱袋,使用时只要把“吸金球”浸入电镀液,过一会提起来,就能“吸”出盐溶液中的金,据上所述,“吸金球”中用于“吸金”物质可能是( )
某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图所示的“吸金球”,“吸金球”是装有一些“吸金”物质的纱袋,使用时只要把“吸金球”浸入电镀液,过一会提起来,就能“吸”出盐溶液中的金,据上所述,“吸金球”中用于“吸金”物质可能是( )| A. | 磁石(主要成分是Fe3O4) | B. | 铁屑(Fe) | ||
| C. | 胆矾(CuSO4•5H2O) | D. | 活性炭(C) |
| A. | 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 | |
| B. | 分子是构成物质的微粒,因此物质都是由分子构成的 | |
| C. | 碱中都含有氢氧根,所以碱中一定含有氢元素 | |
| D. | 铁丝能在氧气中燃烧,空气中有氧气,所以铁丝也能在空气中燃烧 |
| A. | 用小苏打作发酵粉焙制糕点 | B. | 用甲醛溶液浸泡海产品 | ||
| C. | 用工业石蜡给水果上蜡“美容” | D. | 用工业酒精勾兑饮用酒 |
| A. | 植物生长 | B. | 火箭升空 | C. | 水电站发电 | D. | 火力发电 |
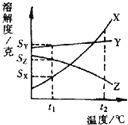
| A. | 当X中含有少量Y时,可用结晶法提纯X | |
| B. | 分别将X、Y、Z的饱和溶液的温度从t2℃降低到t1℃,只有Z无晶体析出 | |
| C. | t2℃时,三种物质的饱和溶液中溶质的质量分数X>Y>Z | |
| D. | t1℃时,用l00克水配制质量与溶质质量分数相同的X、Y、Z的溶液,所需溶质质量最多不超过Sy |