题目内容
10.向盛有10mL稀盐酸(其中滴有少量指示剂)的烧杯中加入氢氧化钠溶液,用pH计测定溶液的pH,所得数据如下.请分析并回答下列问题:| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.5 | 7.0 | 11.0 | 12.0 |
②若滴加的指示剂是紫色石蕊溶液,当加入氢氧化钠溶液的体积为13mL时,溶液显蓝色.
③若滴加的指示剂是无色酚酞溶液,加入氢氧化钠溶液充分振荡后,溶液颜色无变化.此时溶液中的溶质一定有(填化学式)NaCl.
分析 (1)盐酸和氢氧化钠反应生成氯化钠和水,该反应属于复分解反应,可以据此解答该题;
(2)从表格中的数据可以完成该题的解答;
(3)无色酚酞遇碱会变红,而酸性和中性溶液不会变色,可以据此解答该题.
解答 解:(1)盐酸和氢氧化钠反应生成氯化钠和水,该化学方程式为:NaOH+HCl═NaCl+H2O;
(2)根据表格中的数据可以知道当滴入13mL氢氧化钠溶液后溶液的pH大于7,呈碱性,所以加入紫色石蕊试液能够变蓝色;故填:蓝;
(3)滴入一定量氢氧化钠溶液后,酚酞仍为无色,可推断此时的溶液可能含有未反应完的盐酸而呈酸性,或恰好完全反应而呈中性;因此,此时溶液中一定含反应生成的氯化钠.故答案为:NaCl.
点评 盐酸与氢氧化钠反应时,若氢氧化钠量不足时,盐酸过量,则溶液中一定含有盐酸溶质.若氢氧化钠过量时,溶液中的溶质一定有氢氧化钠.但是不管谁过量,反应后的溶液中一定含有氯化钠.

练习册系列答案
相关题目
1.我校某化学兴趣小组的同学到实验室发现,有一瓶配制好的氢氧化钠溶液没有盖上瓶盖.对于该溶液是否变质,小组同学讨论后提出以下猜想:
猜想1:该溶液没有变质
猜想2:该溶液全部变质
猜想3:部分变质
(1)NaOH溶液变质的原因是2NaOH+CO2═Na2CO3+H2O.(用化学方程式表示)
(2)为验证上述猜想,小刘同学取上述NaOH溶液于试管中,滴加足量稀盐酸,有气泡产生.由此说明,猜想1不成立.
(3)为了验证猜想3,小红同学设计了如下实验方案,请你帮她完成实验报告.
(4)实验反思:氢氧化钠必须密封保存.
猜想1:该溶液没有变质
猜想2:该溶液全部变质
猜想3:部分变质
(1)NaOH溶液变质的原因是2NaOH+CO2═Na2CO3+H2O.(用化学方程式表示)
(2)为验证上述猜想,小刘同学取上述NaOH溶液于试管中,滴加足量稀盐酸,有气泡产生.由此说明,猜想1不成立.
(3)为了验证猜想3,小红同学设计了如下实验方案,请你帮她完成实验报告.
| 实验步骤 | 实验现象 | 结论 |
| 取样,向样品中加入过量的氯化钡溶液,过滤 | ①产生白色沉淀 | 猜想3成立 |
| 向上述滤液中滴加几滴无色酚酞溶液 | ②溶液变红 |
19.下列关于铁钉生锈说法不正确的是( )


| A. | ①中的铁钉底部生锈最严重 | |
| B. | ②中的蒸馏水煮沸的目的是除去水中的溶氧 | |
| C. | ②中的植物油是为了隔绝空气 | |
| D. | ①②③对比可探究铁的锈蚀至少与氧气和水有关 |
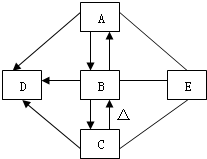 如图A、B、C、D、E是初中化学中常见的五种物质,且A、B、C、D都含有一种相同的元素.其中C俗称小苏打,D为食盐的主要成分,A、E发生中和反应,图中“--”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物或生成物已略去.根据图示关系及所给条件完成下列各空:
如图A、B、C、D、E是初中化学中常见的五种物质,且A、B、C、D都含有一种相同的元素.其中C俗称小苏打,D为食盐的主要成分,A、E发生中和反应,图中“--”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物或生成物已略去.根据图示关系及所给条件完成下列各空: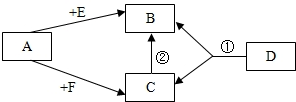 已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.
已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.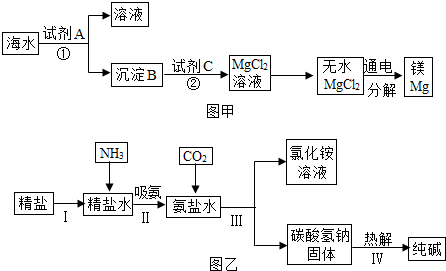
 在公共场所有如下一则广告,请你分析是否科学.
在公共场所有如下一则广告,请你分析是否科学.  如图a、b、c是三种固体物质的溶解度曲线.
如图a、b、c是三种固体物质的溶解度曲线.