题目内容
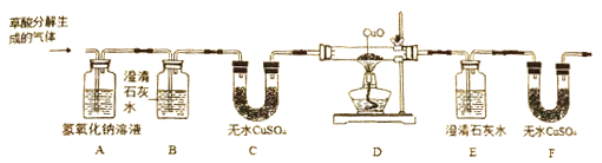
【题目】根据下列实验装置图,回答问题:
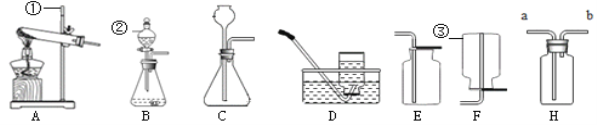
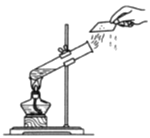
(1)写出装置中带有标号的仪器名称:①_____;②_____;③_____。
(2)若用氯酸钾与二氧化锰混合物制取氧气,应选用的发生装置是_____(填"字母");若要收集到干燥的O2,应选择的收集装置是_____;若用过滤的方法从反应后的剩余固体(MnO2是难溶于水的固体粉末)中回收MnO2,在操作中使用的玻璃仪器除了漏斗和玻璃棒外,还需要_____。
(3)某同学用E装置收集满了一瓶氧气,并用此瓶氧气做铁丝燃烧实验,发现实验现象非常明显,但实验后发现集气瓶底炸裂了,则原因是_____。
(4)实验室常用大理石或石灰石与稀盐酸反应来制取二氧化碳气体,则发生反应的化学方程式为_____;收集二氧化碳气体时,应选择_____(填"字母")装置来收集;发生装置可以选择B或C,其中选择装置B比装置C有明显的优点,其优点是_____;
(5)实验室制取氢气时,常用锌粒和稀硫酸反应,则实验室制取氢气时可以选用_____(填"字母")装置来制取,收集氢气时,除可以用D和F装置收集外,图H装置也常用来收集气体,如用H装置来收集氢气,则气体应从_____(“a”或“b”)进入。
【答案】铁架台 分液漏斗 集气瓶 A E或H 烧杯 集气瓶底部没要放少量的水或细沙,生成物溅落瓶底; CaCO3+2HCl=CaCl2+H2O+CO2↑ E或H 控制反应的速率 BD或BF或CD或CF(合理即可) b
【解析】
(1)装置中带有标号的仪器名称:①是铁架台;②是分液漏斗;③集气瓶;
(2)用氯酸钾与二氧化锰混合物制取氧气,该是反应的反应物是固体,反应条件是加热,应选用的发生装置是A;氧气密度大于空气,不易溶于水,可用向上排空气法收集或排水法收集,用向上排空气法收集的气体较为干燥,若要制取并收集一瓶比较干燥的氧气,应选择的收集装置是E或H;若用过滤的方法从反应后的剩余固体(MnO2是难溶于水的固体粉末)中回收MnO2,在操作中使用的玻璃仪器除了漏斗和玻璃棒外,还需要烧杯;
(3)某同学用E装置收集满了一瓶氧气,并用此瓶氧气做铁丝燃烧实验,发现实验现象非常明显,但实验后发现集气瓶底炸裂了,其原因是集气瓶底部没要放少量的水或细沙,生成物溅落瓶底;
(4)实验室常用大理石或石灰石与稀盐酸反应来制取二氧化碳气体,大理石或石灰石的主要成分是碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳密度大于空气,可用向上排空气法收集,收集二氧化碳气体时,应选择E或H装置来收集;发生装置可以选择B或C,B中分液漏斗能控制液体的滴加速率,从而能控制反应的速率,选择装置B比装置C有明显的优点,其优点是控制反应的速率;
(5)实验室制取氢气时,常用锌粒和稀硫酸反应,该反应的反应物是固体的与液体,不需加热,氢气密度小于空气,难溶于水,可用向下排空气法收集或排水法收集,则实验室制取氢气时可以选用BD或BF或CD或CF装置来制取,收集氢气时,除可以用D和F装置收集外,图H装置也常用来收集气体,氢气死的密度小于空气的,如用H装置来收集氢气,则气体应从b进入。

 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案【题目】以下是教材中关于水的一些实验,根据所学水的知识回答下列问题:
|
|
|
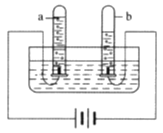
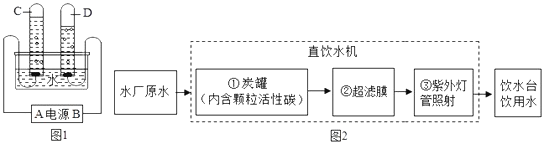
A.水的沸腾 | B.水的电解 | C.水的净化 |
(1)对于实验A中水的沸腾,下列说法正确的是_____(填字母)。
A 水分子之间间隔不变 B 水分子的运动速率加快
C 水分子保持不变 D 保持水化学性质的粒子是氢原子和氧原子
(2)实验B水的电解中试管b得到的气体是_____(填名称)。
(3)实验C中净化水时,小卵石和石英砂的作用是_____。
(4)水是一种重要的化工原料。氯碱工业通过电解饱和氯化钠溶液的方法制取烧碱(NaOH),其中发生的主要反应是氯化钠和水在通电的条件下生成氢氧化钠、氢气、氯气(Cl2),该反应的化学方程式为_____。