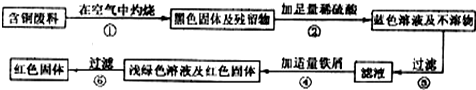
题目内容
20.实验室可利用碱式碳酸铜(化学式:Cu2(OH)2CO3)制备氧化铜,并进行碳粉还原氧化铜的实验.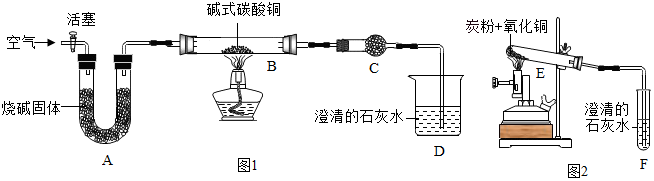
①制备氧化铜并检验产物,装置如图1所示(省略夹持仪器):
步骤一:连接A和B,打开活塞,通入空气.
步骤二:关闭活塞,连上C和D,开始加热.
步骤三:在加热过程中,记录在B中固体质量变化如下表,在t3时停止加热.
| 加热时间(min) | 0 | t1 | t2 | t3 |
| B中固体质量(g) | 6.66 | 5.20 | 4.80 | 4.80 |
A的作用是吸收空气中的水蒸气和二氧化碳,防止对产物检验造成干扰.
②一定量碳粉还原①中制得的氧化铜并检验产物,装置如图2所示:实验过程中,观察到F中溶液变浑浊,E中的现象是黑色粉末变成红色.
分析 ①空气中含有水蒸气和二氧化碳,对制备氧化铜的产物检验造成干扰,据此分析氢氧化钠的作用.
②根据在高温条件下碳能还原氧化铜分析实验的现象.
解答 解:①由于恐怖气中含有水蒸气和二氧化碳,对制备氧化铜的产物检验造成干扰,氢氧化钠能吸收二氧化碳和水蒸气,所以,A的作用是吸收空气中的水蒸气和二氧化碳,防止对产物检验造成干扰.
②由于在高温条件下碳能还原氧化铜生成了铜和二氧化碳,所以,实验过程中,观察到F中溶液变浑浊,E中的现象是 黑色粉末变成红色.
故答为:①水蒸气和二氧化碳;②黑色粉末变成红色.
点评 在解此类题时,首先分析题中各个步骤和反应的作用,然后结合学过的知识和题中所给的条件进行分析解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列各组物质名称和俗称不代表同一物质的一组是( )
| A. | 氯化钠、盐 | B. | 氢氧化钠、苛性钠 | ||
| C. | 碳酸钠、纯碱 | D. | 碳酸氢钠 小苏打 |
12.-些食物的近似pH如下:葡萄3.5--4.5,苹果2.9--3.3,牛奶6.3,--6.6,鸡蛋清7.6--8.0.下列说法错误的是( )
| A. | 胃酸过多的人不应多食苹果 | B. | 葡萄汁能使紫色石蕊试液变蓝 | ||
| C. | 鸡蛋清是碱性食物 | D. | 苹果汁的酸性比葡萄汁强 |
9.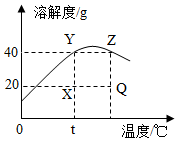 如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是( )
如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是( )
 如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是( )
如图是某固态物质的溶解度曲线,图中的4个点分别表示在某条件下,该溶质的溶液所处的一种状况.下列说法正确的是( )| A. | t℃时该溶质的溶液接近饱和,升温、降温均不能变成饱和溶液 | |
| B. | X、Q点表示溶液的溶质质量分数均为20% | |
| C. | t℃时100g水中最多溶解该物质40g | |
| D. | Y、Z点表示的溶液的溶解度关系是Y<Z |