题目内容
11.某同学在探究学习活动中,测出了家中某些物质的pH:| 物质 | 醋 | 肥皂水 | 食盐水 | 牙膏 |
| pH | 3 | 10 | 7 | 9 |
(2)马蜂的蜂毒是酸性的,若你被马蜂蜇了,可用上述物质中的肥皂水、牙膏涂抹在皮肤上.
(3)日常生活中煤炭燃烧可能产生少量的SO2气体,可用NaOH溶液吸收,该反应的方程式为2NaOH+SO2=Na2SO3+H2O.
分析 (1)根据酸性物质能使石蕊变红色,pH<7的溶液呈酸性解答;
(2)根据肥皂水的pH>7,肥皂水呈碱性可以消耗蚁酸解答;
(3)二氧化硫和氢氧化钠反应生成亚硫酸钠和水;
解答 解:(1)酸性物质能使石蕊变红色,pH<7的溶液呈酸性;醋的pH小于3说明醋呈酸性,
(2)为毒刺显酸性,所以应该涂抹碱性物质,碱性溶液的pH大于7,肥皂水和牙膏的pH大于7,显碱性涂抹在皮肤上可减轻疼痛,理由是肥皂水、牙膏都能中和马蜂的蜂毒中的酸性物质;
(3)二氧化硫和氢氧化钠反应生成亚硫酸钠和水,反应方程式为:2NaOH+SO2=Na2SO3+H2O.
故答案:
(1)醋;
(2)肥皂水、牙膏;
(3)2NaOH+SO2=Na2SO3+H2O.
点评 本题主要考查了溶液与酸碱指示剂相互作用的情况以及酸碱中和反应的相关内容.要记住pH<7的溶液呈酸性;pH=7的溶液呈中性;pH>7的溶液呈碱性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.如图所示试剂瓶标签上的化学式书写错误的是( )
| A. | 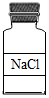 | B. | 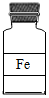 | C. | 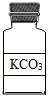 | D. | 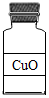 |
9.中科大合肥微尺度物质科学国家实验室谢毅教授、孙永福特任教授课题组设计出一种新型电催化材料,能够将二氧化碳高效“清洁”地转化成液体燃料甲酸,(甲酸的化学式为HCOOH),该成果刊登于2016年1月7日的《自然》杂志.下列有关甲酸说法正确的是( )
| A. | 甲酸由1个碳原子、2个氢原子、2个氧原子构成 | |
| B. | 甲酸属于氧化物 | |
| C. | 甲酸中氧元素的质量分数最大 | |
| D. | 甲酸中碳、氢、氧元素质量比为1:2:2 |
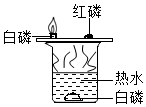 在500mL的烧杯中注入400mL热水,并放入用硬纸圈圈住的一小块白磷,在烧杯上盖一片薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面上水的白磷(如图),回答下列问题:
在500mL的烧杯中注入400mL热水,并放入用硬纸圈圈住的一小块白磷,在烧杯上盖一片薄铜片,铜片上一端放一小堆干燥的红磷,另一端放一小块已用滤纸吸去表面上水的白磷(如图),回答下列问题: 已知A、B、C、D、E、F六种物质间有如图所示的转变关系(发生的反应都是化合反应),其中A、B、C在通常情况下是三种无色无味的气体,且C为化合物,D是一种无色的液体氧化物,F是一种能使紫色石蕊试液变红的物质.
已知A、B、C、D、E、F六种物质间有如图所示的转变关系(发生的反应都是化合反应),其中A、B、C在通常情况下是三种无色无味的气体,且C为化合物,D是一种无色的液体氧化物,F是一种能使紫色石蕊试液变红的物质.