题目内容
1. 小维与家人聚餐时,对火锅燃料“固体酒精”产生了好奇,于是他与同学对其成分进行如下探究.【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
小维与家人聚餐时,对火锅燃料“固体酒精”产生了好奇,于是他与同学对其成分进行如下探究.【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中氢氧化钠是否变质?
【作出猜想】猜想一:酒精中含有碳元素.
猜想二:固体酒精中氢氧化钠已变质.
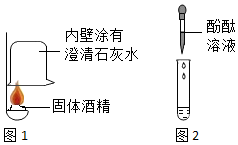
【实验探究】(1)如图1所示进行实验,发现澄清石灰水变浑浊,可得出酒精中含有碳元素的结论.
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现杯底有白色沉淀.取沉淀于试管中加入稀盐酸,固体溶解并有气泡产生,则生成气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
【实验结论】(1)酒精中含有碳元素.
(2)固体酒精中氢氧化钠已经变质.
【拓展延伸】为进一步确定固体酒精中是否还含有氢氧化钠,小维与同学继续探究.
(1)他另取少量固体酒精,加水溶解后,取上层清液,滴加酚酞溶液,酚酞溶液变红色,于是得出固体酒精中还含有氢氧化钠.
(2)小维的同学认为他的实验不能证明固体酒精中一定有氢氧化钠剩余,理由是碳酸钠溶液呈碱性也能使酚酞试液变红.
(3)他们另取上层清液,加入足量的氯化钡溶液,充分反应后滴加氯化铁溶液,生成红褐色沉淀,他们一致认为固体酒精中氢氧化钠有剩余.
【反思交流】(1)实验中,加入足量氯化钡溶液的目的是除去碳酸钠.
(2)实验室中氢氧化钠应密封保存.
分析 根据物质的性质以及物质间反应的实验现象进行分析解答,根据二氧化碳能使澄清的石灰水变浑浊,碳酸钙不溶于水且能与盐酸反应产生二氧化碳气体以及碳酸钠溶液呈碱性进行分析解答即可.
解答 解:【实验探究】(1)酒精中含有碳元素,则燃烧会生成二氧化碳,二氧化碳能使澄清石灰变浑浊,故填:变浑浊.
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现杯底有白色沉淀,说明有不溶于水的物质存在,取沉淀于试管中加入稀盐酸,固体溶解并有气泡产生,说明含有碳酸盐,根据固体酒精的成分,该不溶于的沉淀是氢氧化钠变质生成的碳酸钠与氯化钙反应生成的碳酸钙,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,故填:CaCO3+2HCl═CaCl2+H2O+CO2↑.
【拓展延伸】(1)氢氧化钠的水溶液呈碱性,能使酚酞试液变红,故取少量固体酒精,加水溶解后,取上层清液,滴加酚酞溶液,酚酞溶液变红,故填:变红色;
(2)由于碳酸钠的水溶液呈碱性,也能使酚酞试液变红,故小维的同学认为他的实验不能证明固体酒精中一定有氢氧化钠剩余,故填:碳酸钠溶液呈碱性也能使酚酞试液变红.
【反思交流】(1)实验中,加入足量氯化钡溶液是为了除去碳酸钠,以便检验氢氧化钠是否存在,故填:除去碳酸钠.
(2)由于氢氧化钠容易变质,故实验室中氢氧化钠应密封保存,故填:密封.
点评 本题考查的是变质药品成分的实验探究,完成此题,可以依据已有的知识进行.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
9.二氧化氯消毒液是国际上公认的新一代强力、安全、高效的消毒剂,它能够迅速、彻底杀灭各种细菌和病菌,二氧化氯消毒瓶上的标签如下表.(g取10N/kg)
(1)欲配制30千克质量分数为20%的稀二氧化氯消毒液用来消毒,需要多少千克这种二氧化氯消毒液?
(2)将一个体积为200cm3的铁球浸没在溶质的质量分数为80%的二氧化氯消毒液中,铁球受到的浮力为多少?
| 二氧化氯消毒液1000mL | |
| 溶质的质量分数 | 80% |
| 密度 | 1.2g/cm3 |
| 强腐蚀性,阴冷,密封储存 | |
(2)将一个体积为200cm3的铁球浸没在溶质的质量分数为80%的二氧化氯消毒液中,铁球受到的浮力为多少?
16.下列有关金刚石和石墨的说法中,正确的是( )
| A. | 硬度都比较大 | B. | 都具有良好的导电性 | ||
| C. | 完全燃烧都生成二氧化碳 | D. | 常温下化学性质都活泼 |

