题目内容
(2011?黄埔区一模)颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”.实验室制备的方法是:以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”.请回答以下问题:(1)写出生成“纳米铁”的化学方程式______. Fe+2HCl
【答案】分析:纳米级的单质铁具有很强的反应活性,易与空气中的氧气反应,制取时要使用保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”,根据质量守恒定律,同时能生成氯化氢,要设计实验验证铁、铜、镁、汞的金属活动性顺序,可以依据金属活动性顺序的意义进行,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,且位置越靠前,反应的越剧烈,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答:解:(1)根据题干叙述,以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”,可知同时生成氯化氢,所以本题答案为:FeCl2+H2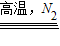 Fe+2HCl;
Fe+2HCl;
(2)纳米级的单质铁具有很强的反应活性,易与空气中的氧气反应,制取时要使用保护气,所以本题答案为:纳米铁有很强的反应活性,防止铁在高温下与氧气反应;
(3)将大小一样的铁片和镁片分别加入到溶质质量分数相同的稀盐酸中,根据实验①判断出镁的金属活动性比铁强,采用的是金属与酸的反应的方式,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,且位置越靠前,反应的越剧烈,现象就是镁片与盐酸反应比铁片与盐酸反应剧烈,将铜片加入到硝酸汞溶液中,铜片上出现银白色物质,说明铜能将汞置换出来,从而证明铜>汞,实验③中的B是蓝色溶液,则金属A是铁,所以本题答案为:镁片与盐酸反应比铁片与盐酸反应剧烈,铜比汞的金属活动性强,铁.
点评:本题考查了金属的有关性质以及金属活动性顺序的应用,同学们要会利用金属活动顺序表设计实验,去验证金属的还原性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
解答:解:(1)根据题干叙述,以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”,可知同时生成氯化氢,所以本题答案为:FeCl2+H2
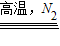 Fe+2HCl;
Fe+2HCl;(2)纳米级的单质铁具有很强的反应活性,易与空气中的氧气反应,制取时要使用保护气,所以本题答案为:纳米铁有很强的反应活性,防止铁在高温下与氧气反应;
(3)将大小一样的铁片和镁片分别加入到溶质质量分数相同的稀盐酸中,根据实验①判断出镁的金属活动性比铁强,采用的是金属与酸的反应的方式,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,且位置越靠前,反应的越剧烈,现象就是镁片与盐酸反应比铁片与盐酸反应剧烈,将铜片加入到硝酸汞溶液中,铜片上出现银白色物质,说明铜能将汞置换出来,从而证明铜>汞,实验③中的B是蓝色溶液,则金属A是铁,所以本题答案为:镁片与盐酸反应比铁片与盐酸反应剧烈,铜比汞的金属活动性强,铁.
点评:本题考查了金属的有关性质以及金属活动性顺序的应用,同学们要会利用金属活动顺序表设计实验,去验证金属的还原性强弱.氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
(2011?黄埔区一模)现有下列仪器:
(1)在过滤操作中需要玻璃棒、______、______等玻璃仪器 (填仪器的名称);
(2)用氯化钠固体配制50g质量分数为5%氯化钠溶液,除了需要用到①和④仪器外,还需要用到的仪器是______、______(用序号填空).
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
 |  |  |  |  |  |  |
(2)用氯化钠固体配制50g质量分数为5%氯化钠溶液,除了需要用到①和④仪器外,还需要用到的仪器是______、______(用序号填空).


