题目内容
16.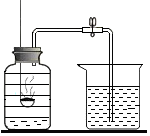 如图在测定空气中氧气的含量实验中,实验现象是:
如图在测定空气中氧气的含量实验中,实验现象是:(1)红磷燃烧,发出黄白色火焰,产生产生大量的白烟;
(2)打开弹簧夹,水压入瓶内,水面上升约$\frac{1}{5}$;文字表达式为磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
属于化合反应(反应类型).
在实际实验中集气瓶内水面上升不足$\frac{1}{5}$,造成的原因可能有:
①没有冷却至室温,就打开弹簧夹
②装置气密性不够好
经过改进最终水面上升到$\frac{1}{5}$,从该现象可得出结论空气中氧气的体积分数大约为$\frac{1}{5}$.
分析 (1)根据磷燃烧的生成物来回答现象;
(2)根据磷燃烧消耗氧气使瓶内压强减小来分析;根据可能造成进入水的体积少的原因进行分析.
解答 解:(1)红磷燃烧生成的五氧化二磷属于白色固体颗粒,所以现象是产生白烟;
(2)由于磷燃烧消耗了氧气使瓶内压强减小,小于外界大气压,在外界大气压的作用下,把水压入瓶内,由于水进入瓶内的体积约占瓶子总体积的五分之一,红磷燃烧生成的五氧化二磷,其反应的文字表达式为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷,反应符合“多变一”的特点,属于化合反应;造成进入水的体积少的原因:装置漏气、红磷量不足没有把瓶内氧气消耗完,没有冷却到室温就打开了止水夹;由于水进入瓶内的体积约占瓶子总体积的五分之一,所以结论是氧气约占空气体积的五分之一;
故答案为:(1)产生大量的白烟;(2)压入瓶内;$\frac{1}{5}$;磷+氧气$\stackrel{点燃}{→}$五氧化二磷;化合;没有冷却至室温,就打开弹簧夹;装置气密性不够好(或红磷量不足;集气瓶中的氧气没有消耗完);空气中氧气的体积分数大约为$\frac{1}{5}$.
点评 根据实验操作图,回忆实验中现象,从而理解该实验的目的和获得的结论.在推算氮气的性质时要根据实验的现象来进行分析.

练习册系列答案
相关题目
7.下列物质的用途中,主要利用其化学性质的是( )
| A. | 铜丝做导线 | B. | 液氮用作制冷剂 | ||
| C. | 液氢可作航空燃料 | D. | 铁制铁锅 |
11.下列关于空气各成分的说法中,正确的是( )
| A. | 氧气的化学性质比较活泼,能够燃烧 | |
| B. | 空气中氮气的质量分数为78% | |
| C. | 稀有气体都不能与物质发生化学反应 | |
| D. | 氮气的化学性质不活泼,可用于食品防腐 |
1.学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜(CuO)能否起到类似二氧化锰的催化剂作用呢?于是进行了以下探究.
【猜想】:
Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】
用天平称量0.2g氧化铜(CuO),取5mL5%的过氧化氢溶液于试管中,进行如图1实验:
(1)填写下表:
(2)步骤①的目的是与步骤③对照.
(3)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(4)同学通过查阅资料得知,过氧化氢在70℃以上会较快分解产生氧气.为了验证加热过氧化氢也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生大量气泡,但将带火星的木条放在导管口没有复燃,可能的原因是放出的氧气中含有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
【猜想】:
Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】
用天平称量0.2g氧化铜(CuO),取5mL5%的过氧化氢溶液于试管中,进行如图1实验:

(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 | |
| 溶液中有气泡放出, 带火星的木条复燃. | 称量的氧化铜的质量 仍为0.2g | 溶液中有气泡放出 带火星的木条复燃 | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立. | |
(3)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为过氧化氢$\stackrel{氧化铜}{→}$水+氧气.
(4)同学通过查阅资料得知,过氧化氢在70℃以上会较快分解产生氧气.为了验证加热过氧化氢也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实验中观察到试管内产生大量气泡,但将带火星的木条放在导管口没有复燃,可能的原因是放出的氧气中含有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
8.现有①石油②石墨③矿泉水④铁⑤氯酸钾⑥水.对上述物质的分类正确的是( )
| A. | 混合物--①②③ | B. | 氧化物--⑤⑥ | C. | 单质--②④ | D. | 化合物--③⑤ |
6.人体缺乏碘元素会引起的病症是( )
| A. | 贫血 | B. | 甲状腺肿大 | C. | 佝偻病 | D. | 夜盲症 |
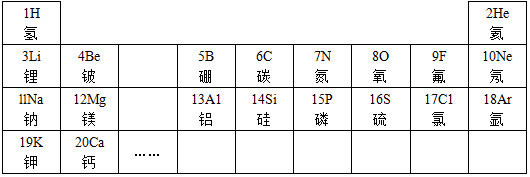
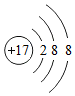 表示的是(填名称)氯离子;
表示的是(填名称)氯离子;