题目内容
9.利用化学知识解释一些现象.(1)为保证安全,进入久未开启的菜窖前,必须先做灯火实验.
(2)防毒面具的滤毒罐里盛放活性炭,这是利用了活性炭的吸附性.
(3)已知含Ba2+的溶液会使人中毒,胃镜透视时通常服用“钡餐”,其成分是BaSO4而不能用BaCO3,这是由于(用化学方程式解释)BaCO3+2HCl=BaCl2+H2O+CO2↑.
(4)曾青得铁则化为铜指的是(用化学方程式解释)Fe+CuSO4═FeSO4+Cu.
分析 (1)根据二氧化碳的性质分析;
(2)根据活性炭具有吸附性分析回答;
(3)根据胃液中的盐酸能与碳酸钡反应分析回答;
(4)根据铁与硫酸铜的反应分析回答.
解答 解:(1)由于二氧化碳不不能供给呼吸,密度比空气大不燃烧不支持燃烧,为保证安全,进入久未开启的菜窖前,必须先做灯火实验
(2)防毒面具的滤毒罐里盛放活性炭,这是利用了活性炭的吸附性.
(3)人体胃液中含有一定量盐酸,盐酸能与碳酸钡反应生成氯化钡、水和二氧化碳,反应的化学方程式为:BaCO3+2HCl=BaCl2+H2O+CO2↑.
(4)曾青得铁则化为铜中的曾青是说的铜的化合物,即用铁将铜的化合物中的铜元素置换出来,反应物是铁和硫酸铜,生成物是硫酸亚铁和铜,所以方程式是:Fe+CuSO4═FeSO4+Cu.
故答为:(1)灯火;(2)防吸;(3)BaCO3+2HCl=BaCl2+H2O+CO2↑;(4)Fe+CuSO4═FeSO4+Cu.
点评 本题的难度不大,考查的知识属于课本的基础知识,根据已有的知识分析解答.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
19.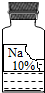 实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂溶质是什么?
【交流研讨】根据受损标签的情况判断,这瓶试剂不可能是A(填字母序号).
A.酸 B.碱 C.盐
【查阅资料】①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
②Na2CO3、NaHCO3溶液都呈碱性.NaCl溶液呈中性.
③室温下(20℃)时,4种物质的溶解度的数据如下.
【分析】小华根据试剂瓶上标注和上表溶解度数据判断,这瓶试剂不可能是NaHCO3.
【猜想与实验】①可能是Na2CO3溶液; ②可能是NaOH溶液; ③可能是NaCl溶液.
(1)小亮用洁净的玻璃棒蘸取该溶液,滴到干燥的pH试纸上,测得pH=11,他判断该溶液不可能是NaCl溶液.
(2)小强为了确定该溶液的成分,进行了如下实验.
【质疑】小华则不同意小强的观点,认为溶液中有Na2CO3还可能有NaOH.小华又进行了以下探究:
【反思与评价】
在小华的探究中,小洋提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案是否可行,并说明理由不可行,因为氢氧化钙与碳酸钠反应会生成氢氧化钠,这样无法确定步骤二的实验结论,也得不出氢氧化钠部分变质的结论.
【理解与应用】
(1)氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例:浓硫酸.
(2)取上述瓶中溶液50克,向其中加入足量的氢氧化钡溶液,完全反应后得到1.97克白色沉淀,求上述溶液中碳酸钠的质量分数.(写出计算过程)
 实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.
实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,是初中化学常用的试剂.小华等几位同学很感兴趣,决定对其成分进行探究.【提出问题】这瓶试剂溶质是什么?
【交流研讨】根据受损标签的情况判断,这瓶试剂不可能是A(填字母序号).
A.酸 B.碱 C.盐
【查阅资料】①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3.
②Na2CO3、NaHCO3溶液都呈碱性.NaCl溶液呈中性.
③室温下(20℃)时,4种物质的溶解度的数据如下.
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【猜想与实验】①可能是Na2CO3溶液; ②可能是NaOH溶液; ③可能是NaCl溶液.
(1)小亮用洁净的玻璃棒蘸取该溶液,滴到干燥的pH试纸上,测得pH=11,他判断该溶液不可能是NaCl溶液.
(2)小强为了确定该溶液的成分,进行了如下实验.
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样品于试管中, 滴加足量稀盐酸 | 有有气泡冒出 | 猜想①正确,发生反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
| 步骤 | 现象 | 结论 |
| 步骤一:取样品于试管中,向其中滴加足量的CaCl2溶液并过滤 | 有白色沉淀生成 | 溶液中既含Na2CO3,又含有NaOH |
| 步骤二:向上述滤液中滴加酚酞试液 | 溶液变红色 |
在小华的探究中,小洋提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案是否可行,并说明理由不可行,因为氢氧化钙与碳酸钠反应会生成氢氧化钠,这样无法确定步骤二的实验结论,也得不出氢氧化钠部分变质的结论.
【理解与应用】
(1)氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例:浓硫酸.
(2)取上述瓶中溶液50克,向其中加入足量的氢氧化钡溶液,完全反应后得到1.97克白色沉淀,求上述溶液中碳酸钠的质量分数.(写出计算过程)
20.分类法是化学上研究物质的常用方法,从物质分类的角度看,下列物质与二氧化碳、二氧化硫、氧化铜属于同一类别物质的是( )
| A. | Ca(OH)2 | B. | Na2CO3 | C. | CH3OH | D. | Fe2O3 |
4.兴趣小组的同学在实验室用澄清石灰水和碳酸钠溶液来制取氢氧化钠溶液.
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,有白色沉淀生成,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”为此,他进行了如下实验:
小妮认为小欢的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是碳酸钠溶液也能使无色酚酞试液变红.
小妮设计了另一个实验:
我认为:小欢和小妮的实验是为了证实小京结论的可靠性,小京的结论不可靠,原因是没有证明有氢氧化钠生成.
显然小妮的实验可靠性比小欢的实验好,原因是排除了干扰因素.
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,有白色沉淀生成,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”为此,他进行了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有氢氧化钠 |
小妮设计了另一个实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,加入足量的BaCl2溶液 | 有白色沉淀生成,过滤,在滤液中滴加几滴无色酚酞溶液,酚酞溶液变红 | 无色溶液中确实含有氢氧化钠 |
显然小妮的实验可靠性比小欢的实验好,原因是排除了干扰因素.
11.下列对实验对象的描述,正确的是( )
| A. | 硫在氧气中燃烧,产生微弱的淡蓝色火焰 | |
| B. | 电解水时与正极相连的一端产生的气体体积是负极的2倍 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 红磷在空气中燃烧,产生大量烟雾,生成P2O5 |