题目内容
16.某KNO3样品中含有少量K2CO3,其提纯流程如下: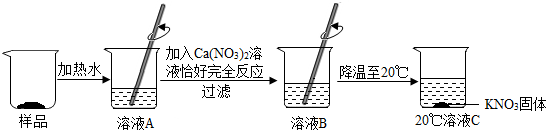
(1)溶液A加入适量Ca(NO3)2溶液,与溶液中K2CO3恰好完全反应,生成CaCO3沉淀和KNO3,写出该反应的化学方程式:Ca(NO3)2+K2CO3=CaCO3↓+2KNO3.
(2)操作a的名称是过滤.
(3)20℃时溶液C是饱和溶液(填“饱和溶液”或“不饱和溶液”).
分析 (1)硝酸钙和碳酸钾反应生成白色沉淀碳酸钙和硝酸钾;
(2)操作a的名称是过滤,通过过滤把液体和固体分离;
(3)条件不变时,析出晶体后的溶液是该溶质的饱和溶液.
解答 解:(1)溶液A加入适量Ca(NO3)2溶液,与溶液中K2CO3恰好完全反应,生成CaCO3沉淀和KNO3,该反应的化学方程式为:Ca(NO3)2+K2CO3=CaCO3↓+2KNO3.
故填:Ca(NO3)2+K2CO3=CaCO3↓+2KNO3.
(2)操作a的名称是过滤,通过过滤把碳酸钙从硝酸钾溶液中分离出来.
故填:过滤.
(3)20℃时溶液C中析出硝酸钾晶体,析出硝酸钾晶体后的溶液是硝酸钾的饱和溶液.
故填:饱和溶液.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
6.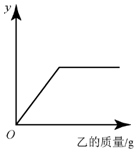 向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )
向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )
 向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )
向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )| 选项 | 甲 | 乙 | y |
| A | Zn | 稀硫酸 | 生成气体的质量 |
| B | NaOH溶液 | FeCl3溶液 | 混合后溶液的质量 |
| C | Al2O3 | 稀盐酸 | 生成水的质量 |
| D | CaCl2溶液 | Na2CO3 | 生成沉淀的质量 |
| A. | A | B. | B | C. | C | D. | D |
7.氯化镁是制取镁的原料之一,现要测定某化工产品(含MgCl2和KCl)中所含的氯化镁质量分数,进行实验:先将10g样品完全溶于水,然后把50g一定质量分数的氢氧化钾溶液平均分五次加入样品溶液中,充分振荡,实验所得数据如表:
请分析上述数据,回答下列问题
(1)表中a为1.16.
(2)样品中的氯化钾属于化肥中的钾肥,可回收利用.
(3)计算样品中氯化镁的质量分数是多少?(写出计算过程)
| 编号 | 1 | 2 | 3 | 4 | 5 |
| 加入氢氧化钾溶液的质量/g | 10 | 10 | 10 | 10 | 10 |
| 生成沉淀的质量/g | 0.58 | a | 1.74 | 2.32 | 2.32 |
(1)表中a为1.16.
(2)样品中的氯化钾属于化肥中的钾肥,可回收利用.
(3)计算样品中氯化镁的质量分数是多少?(写出计算过程)
4.下列4个图象能正确反映对应的实验操作的是( )
| A. | 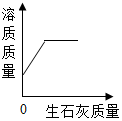 向一定量的饱和Ca(OH)2溶液中加入一定量的生石灰 | |
| B. | 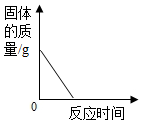 向一定量的CuO中通入CO气体并加热 | |
| C. | 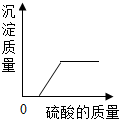 向一定量的KOH和Ba(NO3)2的混合溶液中,逐滴加入稀H2SO4 | |
| D. | 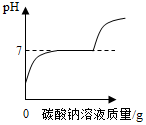 向一定量的HCl和CaCl2(CaCl2溶液呈中性)的混合液中加入Na2CO3溶液 |
11.分子和原子的主要区别是( )
| A. | 分子是构成物质的微粒,原子不是构成物质的微粒 | |
| B. | 分子由原子构成,所以分子的质量都大于原子质量 | |
| C. | 分子在不停地运动,原子在分子中不可能运动 | |
| D. | 分子在化学反应中可分,原子在化学反应中不可再分 |
1.甲醛(CH2O)是室内装潢所产生的主要污染物之一. 下列说法正确的是( )
| A. | 它是由碳、氢、氧三种元素组成的 | |
| B. | 它是由碳原子和水分子构成 | |
| C. | 它的一个分子是由一个碳原子、一个氢分子和一个氧原子构成的 | |
| D. | 它是由一个碳元素、两个氧元素和一个氧元素组成 |
8.下列实验方案中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去生石灰中含有的杂质石灰石 | 先加足量水,然后过滤 |
| B | 除去硫酸钾固体中的少量碳酸钾粉末 | 加入适量稀硫酸充分反应,蒸发、结晶 |
| C | 分离硫酸钠和硫酸铜的混合溶液 | 加入过量氢氧化钠溶液后过滤,将滤渣溶于稀硫酸 |
| D | 区分MnO2和CuO两种固体粉末 | 用观察物质颜色的方法进行区分 |
| A. | A | B. | B | C. | C | D. | D |
5. 如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
 如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )| X | Y | |
| A | CO2 | Ca(OH)2 |
| B | CO | NaOH |
| C | HCl | Ca(OH)2 |
| D | SO2 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
