题目内容
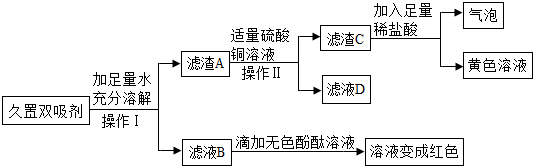
8.A、B、C、D为初中化学常见的化合物,它们是由H、C、O、Na、Cl、Ca中的两种或三种元素组成,相对分子质量均小于100.(1)取少量A的无色溶液,滴加石蕊试液,溶液呈蓝色.A的水溶液显碱性.
(2)向上述溶液中通入足量的气体B,无浑浊现象,且反应后溶液仍为蓝色.该反应的化学方程式为CO2+2NaOH=Na2CO3+H2O.
(3)向(2)所得溶液中加入一定量C的溶液,出现浑浊现象.过滤后,滤液仍为蓝色.由此推断,
C物质是Ca(OH)2(写化学式),产生浑浊现象的原因是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(用化学方程式表示).
(4)向滤液中加入一定量D溶液,没有气泡产生,反应后溶液变为红色.由此推断,D物质是HCl
(写化学式),最后得到的溶液中溶质(指示剂除外)可能是NaCl、HCl或NaCl、CaCl2、HCl(写出所有可能).
分析 根据提供的元素以及元素能组成的物质、物质的性质进行分析解答即可.
解答 解:(1)取少量A的无色溶液,滴加石蕊试液,溶液呈蓝色,说明A的溶液呈碱性.故填:碱;
(2)溶液中通入足量的气体B,无浑浊现象,且反应后溶液仍为蓝色,说明是将二氧化碳通入氢氧化钠溶液中生成了碳酸钠和水,故填:CO2+2NaOH=Na2CO3+H2O;
(3)氢氧化钙能与碳酸钠反应生成碳酸钙沉淀,同时生成氢氧化钠,故填:Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(4)向滤液中加入一定量D溶液,没有气泡产生,反应后溶液变为红色,说明加入了过量的酸溶液,故D是盐酸,由于盐酸过量,故一定含有盐酸,盐酸能与氢氧化钠反应生成氯化钠,能与碳酸钙反应生成氯化钙,若是氢氧化钙与碳酸钠恰好反应或是碳酸钠剩余,则含有盐酸和氯化钠,若是氢氧化钙剩余则含有盐酸、氯化钠和氯化钙,故填:HCl; NaCl、HCl或NaCl、CaCl2、HCl.
点评 掌握常见的物质的性质以及物质间反应的实验现象是正确解答本题的关键.

练习册系列答案
相关题目
3.如图表示了绿色植物光合作用的主要过程,下列说法不正确的是( )


| A. | X是O2 | |
| B. | C6H12O6是有机物 | |
| C. | C6H12O6与X反应生成CO2和H2O属于置换反应 | |
| D. | 绿色植物通过光合作用,将太阳能转化成化学能 |
13.粗盐提纯的实验中,下列图示操作不正确的是( )
| A. | 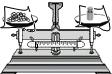 称量 | B. | 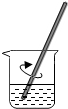 溶解 | C. | 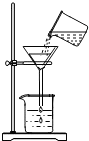 过滤 | D. | 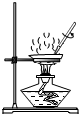 蒸发 |
17.化学是在分子、原子、离子水平上研究物质及其变化的科学.
(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图所示.下列说法正确的是BE(选填字母).
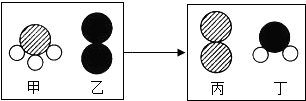
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(2)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异.
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同).
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.
则铝碳酸镁起抗酸作用的两种微粒是OH-;、CO32-.
(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图所示.下列说法正确的是BE(选填字母).

A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(2)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同).
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.
则铝碳酸镁起抗酸作用的两种微粒是OH-;、CO32-.