题目内容
11.实验用NaCl和水配制50g溶质质量分数为5%的NaCl溶液,下列叙述正确的是( )| A. | 称量NaCl时,把它放在托盘天平的右盘 | |
| B. | 将量取的50 mL水,倒入盛有NaCl的烧杯中 | |
| C. | 将配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签 | |
| D. | 实验中用到的玻璃仪器有量筒、烧杯、漏斗和玻璃棒 |
分析 A、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断.
B、利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
C、根据根据配制溶质质量分数一定的溶液的基本步骤,进行分析判断.
D、实验室配制50g5%的NaCl溶液操作步骤分别是:计算、称量、溶解,根据各操作所需要使用的仪器即可.
解答 解:A、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,故选项说法错误.
B、溶质质量=溶液质量×溶质的质量分数,配制50g溶质质量分数为5%的NaCl溶液,需氯化钠的质量=50g×5%=2.5g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-2.5g=47.5g(47.5mL),故选项说法错误.
C、将配好的溶液装入试剂瓶中,盖好瓶塞并贴上标签,故选项说法正确.
D、托盘天平用于称取固体氯化钠、量筒与胶头滴管用于准确量取水、烧杯用于完成溶解操作、玻璃棒用于溶解时的搅拌,其中用到的玻璃仪器有量筒、烧杯和玻璃棒,无需使用漏斗,故选项说法错误.
故选:C.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键.

练习册系列答案
相关题目
1.通过近期的学习,我们已经了解了常见金属的活动性顺序.铬(Cr)是重要的金属材料,在生产、生活中应用广泛.小华想金属活动顺序中没有铬,他和化学兴趣小组的同学们一起对Cr、Al、Cu的金属活动性顺序的相对位置进行了探究,过程如下:
【提出假设】根据已有的知识,对三种金属的活动性顺序提出了三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.Al>Cu>Cr.
【进行实验】取厚薄、形状、体积、大小完全相同,且用砂纸打磨过的三种金属薄片,然后分别 放入试管中,再分别倒入10mL等浓度的足量稀盐酸,观察现象,记录如下:
上述实验使用等浓度的盐酸溶液的理由是盐酸的浓度不同,会影响反应产生的气体的速率.
【得出结论】原假设中正确的是:a(填假设中a、b或c),写出铬与盐酸反应的化学方程式(铬与盐酸反应后显+2价):Cr+2HCl═CrCl2+H2↑.
【反思与评价】同学们认为只用三种药品也可以证明这三种金属的活动性顺序,这三种药品是铬、AlCl3溶液、CuCl2 溶液(或铬、Al2(SO4)3溶液、CuCl2 溶液,
或铝、铜、CrCl2溶液)(只需填写药品的一种组合方案即可).
【结论应用】根据探究结果,在CuCl2和A1C13的混合液中加入一定量的金属铬粉末,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有溶质的化学式是AlCl3、CrCl2.
【提出假设】根据已有的知识,对三种金属的活动性顺序提出了三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c.Al>Cu>Cr.
【进行实验】取厚薄、形状、体积、大小完全相同,且用砂纸打磨过的三种金属薄片,然后分别 放入试管中,再分别倒入10mL等浓度的足量稀盐酸,观察现象,记录如下:
| 金属 | Cr | A1 | Cu |
| 与盐酸发生反应的现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生激烈,金属迅速溶解 | 无明显现象 |
【得出结论】原假设中正确的是:a(填假设中a、b或c),写出铬与盐酸反应的化学方程式(铬与盐酸反应后显+2价):Cr+2HCl═CrCl2+H2↑.
【反思与评价】同学们认为只用三种药品也可以证明这三种金属的活动性顺序,这三种药品是铬、AlCl3溶液、CuCl2 溶液(或铬、Al2(SO4)3溶液、CuCl2 溶液,
或铝、铜、CrCl2溶液)(只需填写药品的一种组合方案即可).
【结论应用】根据探究结果,在CuCl2和A1C13的混合液中加入一定量的金属铬粉末,充分反应后过滤,向滤出的固体中加入盐酸,无明显现象,则滤液中一定含有溶质的化学式是AlCl3、CrCl2.
2.2015年10月5日浙江绍兴一化工厂因硝基氯苯车间反应引起爆炸.硝基氯苯化学式C6H4ClNO2,关于硝基氯苯的说法正确的是( )
| A. | 硝基氯苯中氢元素的质量分数比氮元素大 | |
| B. | 硝基氯苯是由碳、氢、氯、氮、氧五种元素组成 | |
| C. | 硝基氯苯是属于氧化物 | |
| D. | 硝基氯苯是由6个碳原子、4个氢原子、1个氯原子、1个氮原子和2个氧原子构成 |
19.“84消毒液”的有效成分次氯酸钠(NaClO)中,氯元素的化合价为( )
| A. | -1 | B. | +1 | C. | +5 | D. | +7 |
6.根据你的生活经验和所学知识,判断下列做法不能达到目的是( )
| A. | 用食盐水除去水垢 | |
| B. | 用肥皂水鉴别硬水和软水 | |
| C. | 用含氢氧化铝的药物治疗胃酸过多 | |
| D. | 用在空气中灼烧的方法鉴别黄铜和黄金 |
20.在X+Y→盐+水的反应中,X和Y不可能是( )
| A. | NaOH和HCl | B. | Fe2O3和HCl | C. | BaCl2和H2SO4 | D. | NaOH和CO2 |
1.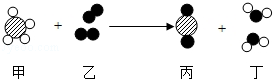 如图为某反应的微观示意图,其中不同的球代表不同的原子.下列说法错误的是( )
如图为某反应的微观示意图,其中不同的球代表不同的原子.下列说法错误的是( )
 如图为某反应的微观示意图,其中不同的球代表不同的原子.下列说法错误的是( )
如图为某反应的微观示意图,其中不同的球代表不同的原子.下列说法错误的是( )| A. | 生成物可能都是氧化物 | |
| B. | 乙中元素的化合价在反应前后保持不变 | |
| C. | 生成物的分子个数比为1:1 | |
| D. | 反应前后原子的种类和数目都不变 |
 如图所示都是常见的日常生活用品,其中是有机高分子材料的有:③⑥(填序号).生活中要鉴别羊毛衫和合成纤维,可通过燃烧法的方法.
如图所示都是常见的日常生活用品,其中是有机高分子材料的有:③⑥(填序号).生活中要鉴别羊毛衫和合成纤维,可通过燃烧法的方法.