题目内容
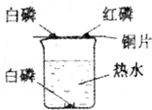
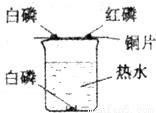
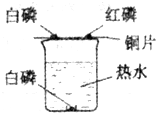 (I)探究燃烧条件的实验装置如下图所示.
(I)探究燃烧条件的实验装置如下图所示.(1)由该实验得,可燃物燃烧的条件是:①
跟氧气(O2或空气)接触
跟氧气(O2或空气)接触
;②温度达到着火点
温度达到着火点
.(2)实验中发生反应的化学方程式为
4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
.
| ||
(3)实验中使用铜片,是利用了铜的
导热性
导热性
.(II)(1)磁铁矿的主要成分是:
Fe3O4
Fe3O4
;(填化学式)(2)写出CO与Fe2O3在高温条件下反应的化学方程式:
Fe2O3+3CO
2Fe十3CO2
| ||
Fe2O3+3CO
2Fe十3CO2
;
| ||
(3)高炉炼铁得到的主要产品是
B
B
;(填序号)A.纯铁B.生铁C.钢(4)铁生锈的主要条件是铁与水和
氧气
氧气
直接接触.分析:(I)(1)依据燃烧的条件进行分析.
(2)依据白磷燃烧的实际分析解决.
(3)根据铜片的物理性质分析解决.
(II)(1)依据磁铁矿的成分解决.
(2)依据一氧化碳能够还原氧化铁并生成铁的事实解决.
(3)依据高炉炼铁的原料进行分析.
(4)依据铁生锈的条件分析判断.
(2)依据白磷燃烧的实际分析解决.
(3)根据铜片的物理性质分析解决.
(II)(1)依据磁铁矿的成分解决.
(2)依据一氧化碳能够还原氧化铁并生成铁的事实解决.
(3)依据高炉炼铁的原料进行分析.
(4)依据铁生锈的条件分析判断.
解答:解:(I)(1)依据燃烧的条件可知可燃物的燃烧要具备两个条件:①跟氧气(O2或空气)接触 ②温度达到着火点;
(2)白磷燃烧时会生成五氧化二磷的白色固体,其方程式为:4P+5O2
2P2O5
(3)铜片上的白磷与红磷是进行对比试验,白磷燃烧红磷不燃烧,从而说明温度对燃烧的影响,其中的铜片能导热可以把热量由水蒸气传递给可燃物.
(II)(1)磁铁矿的主要成分是四氧化三铁化学式为:Fe3O4.
(2)一氧化碳能够还原氧化铁并生成铁和二氧化碳,其方程式为:Fe2O3+3CO
2Fe十3CO2.
(3)高炉炼铁的原料生铁不是纯铁或钢.
(4)铁生锈的条件是与水及氧气接触.
故答案为:(Ⅰ)(1)跟氧气(O2或空气)接触 温度达到着火点(2)4P+5O2
2P2O5(3)导热性
(Ⅱ)(1)Fe3O4(2)Fe2O3+3CO
2Fe十3CO2(3)B(4)氧气
(2)白磷燃烧时会生成五氧化二磷的白色固体,其方程式为:4P+5O2
| ||
(3)铜片上的白磷与红磷是进行对比试验,白磷燃烧红磷不燃烧,从而说明温度对燃烧的影响,其中的铜片能导热可以把热量由水蒸气传递给可燃物.
(II)(1)磁铁矿的主要成分是四氧化三铁化学式为:Fe3O4.
(2)一氧化碳能够还原氧化铁并生成铁和二氧化碳,其方程式为:Fe2O3+3CO
| ||
(3)高炉炼铁的原料生铁不是纯铁或钢.
(4)铁生锈的条件是与水及氧气接触.
故答案为:(Ⅰ)(1)跟氧气(O2或空气)接触 温度达到着火点(2)4P+5O2
| ||
(Ⅱ)(1)Fe3O4(2)Fe2O3+3CO
| ||
点评:此题是一道多点知识的考查题,解题的关键是对各相关基础知识的掌握与了解,以识记的知识为主.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
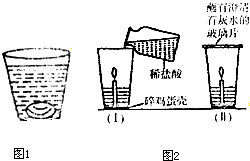 生活中处处有化学,小强把学到的化学知识用于生活中,进行下列探究.
生活中处处有化学,小强把学到的化学知识用于生活中,进行下列探究.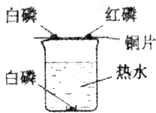 (I)探究燃烧条件的实验装置如下图所示.
(I)探究燃烧条件的实验装置如下图所示.