题目内容
5.如图是通过白磷燃烧来验证质量守恒定律的实验,下列说法错误的是( )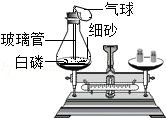
| A. | 白磷燃烧结束,锥形瓶应冷却到室温后再放在天平上称量 | |
| B. | 瓶底的细砂起隔热作用 | |
| C. | 实验过程中气球先变大后变瘪 | |
| D. | 反应前锥形瓶内白磷和氧气的总质量一定等于反应后生成五氧化二磷的质量 |
分析 参加化学反应的物质质量之和,一定等于反应后生成的各种物质质量之和.
解答 解:A、白磷燃烧结束,锥形瓶应冷却后再放在天平上称量,该选项说法正确;
B、瓶底的细砂起隔热作用,该选项说法正确.
C、白磷燃烧放出热量,锥形瓶中的气体膨胀,冷却后气体收缩,因此实验过程中气球先变大后变瘪,该选项说法正确;
D、锥形瓶内的白磷和氧气不一定恰好完全反应,如果恰好完全反应,则反应前锥形瓶内白磷和氧气的总质量一定等于反应后生成五氧化二磷的质量,如果不是恰好完全反应,则反应前锥形瓶内白磷和氧气的总质量一定大于反应后生成五氧化二磷的质量,该选项说法错误;
故选:D.
点评 化学反应前后,元素种类不变,原子种类、总个数不变,这是书写化学方程式和进行相关方面计算的基础.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
1.下列实验操作正确的是( )
| A. | 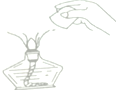 | B. | 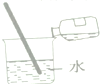 稀释浓H2SO4 | C. | 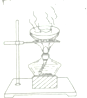 | D. |  称量固体 |
13.科学家以四氯化碳(CCl4)和金属钠为原料,在700℃时制造出纳米级金刚石粉末,该反应的化学方程式为:CCl4+4Na═C(金刚石)+4NaCl.下列说明正确的是( )
| A. | CCl4属于有机化合物 | B. | 该反应为复分解反应 | ||
| C. | 金刚石和石墨是同种物质 | D. | 反应中原子种类发生了变化 |
17.如表为我国《生活饮用水国家标准》的部分内容,请回答下列问题.
(1)测得某地区合格饮用水的pH=6.6,通常是因为水中有一种常见弱酸是H2CO3(填化学式).
(2)生活饮用水中的铝元素以铝离子形式存在,则3个铝离子表示为3Al3+;,铁元素以硫酸铁形式存在,硫酸铁的化学式为Fe2(SO4)3.
(3)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是蒸馏.
(4)天然水的硬度较大时,煮沸后饮用是降低硬度的方法之一,其化学原理是Ca(HCO3)2、Mg(HCO3)2加热后发生反应生成了水垢.因而水垢的主要成分有2种,请写出用醋酸(用HAc代表醋酸,醋酸在水溶液中解离出H+和醋酸根离子Ac-)除去水垢的其中一个反应的化学方程式CaCO3+2HAc=Ca(Ac)2+CO2↑+H2O.
(5)1升合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量应不超过180mg.
| 项目 | 现值 |
| 色度 | 不超过15度 并不得呈现其他异色 |
| 浑浊度 | 不超过1度 特殊情况下不超过5度 |
| pH | 6.5-8.5 |
| 总硬度 | (以CaCO3计)450mg/L |
| 铝 | 0.2mg/L |
| 铁 | 0.3mg/L |
| 硫酸盐 | 250mg/L |
(2)生活饮用水中的铝元素以铝离子形式存在,则3个铝离子表示为3Al3+;,铁元素以硫酸铁形式存在,硫酸铁的化学式为Fe2(SO4)3.
(3)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是蒸馏.
(4)天然水的硬度较大时,煮沸后饮用是降低硬度的方法之一,其化学原理是Ca(HCO3)2、Mg(HCO3)2加热后发生反应生成了水垢.因而水垢的主要成分有2种,请写出用醋酸(用HAc代表醋酸,醋酸在水溶液中解离出H+和醋酸根离子Ac-)除去水垢的其中一个反应的化学方程式CaCO3+2HAc=Ca(Ac)2+CO2↑+H2O.
(5)1升合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量应不超过180mg.
14.物质的性质决定物质的用途,下列物质的用途中只利用了物质的化学性质的是( )
| A. | 二氧化碳灭火 | B. | 金刚石制玻璃刀 | ||
| C. | 铝制高压锅 | D. | 氮气用于食品防腐 |