题目内容
20.现电解36g的水,通电后完全分解,试计算:(1)该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
(2)可制得氢气的质量为多少?
(3)可制得氧气的质量为多少?
分析 电解水生成氢气和氧气,根据水的质量可以计算生成氢气和氧气的质量.
解答 解:设生成氢气和氧气的质量为x、y,
2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,
36 4 32
36g x y
$\frac{36}{36g}$=$\frac{4}{x}$=$\frac{32}{y}$,
x=4g,y=32g,
故答案为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,生成氢气和氧气的质量分别是4g、32g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
10.铁、铜和银是日常生活中经常接触到的三种金属.
(1)三种金属共同具有的物理性质是导热性(或导电性、延展性等)(写出一条即可).
(2)若要证明铁、铜和银的活动性顺序,需要进行的实验有ABD(填序号).
(3)氧化铁是一种红褐色的固体粉末.请根据图1回答问题.

①写出气体X与氧化铁反应的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②Y溶液中的溶质为CuSO4(或CuCl2)和H2SO4(或HCl).
③写出生成无色气体E的化学方程式Fe+H2SO4═FeSO4+H2↑(或Fe+2HCl═FeCl2+H2↑).
(4)根据铁与硫酸铜溶液的反应判断,下表中x和y所表示的四种关系符合图2变化规律的是D(填序号).
(1)三种金属共同具有的物理性质是导热性(或导电性、延展性等)(写出一条即可).
(2)若要证明铁、铜和银的活动性顺序,需要进行的实验有ABD(填序号).
| A.将铁片放入盐酸中 | B.将铜片放入盐酸中 |
| C.将铁片放入硝酸银溶液中 | D.将铜片放入硝酸银溶液中 |

①写出气体X与氧化铁反应的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②Y溶液中的溶质为CuSO4(或CuCl2)和H2SO4(或HCl).
③写出生成无色气体E的化学方程式Fe+H2SO4═FeSO4+H2↑(或Fe+2HCl═FeCl2+H2↑).
(4)根据铁与硫酸铜溶液的反应判断,下表中x和y所表示的四种关系符合图2变化规律的是D(填序号).
| 选项 | x | y |
| A | 铁粉质量 | 溶液质量 |
| B | 铁粉质量 | 析出铜的质量 |
| C | 反应时间 | 生成硫酸亚铁的质量 |
| D | 反应时间 | 反应过程中金属质量的变化情况 |
8.下列关于分子和原子的说法正确的是( )
| A. | 分子是保持物质性质的最小粒子 | B. | 原子是化学变化中的最小粒子 | ||
| C. | 分子的质量不一定比原子的质量大 | D. | 分子是构成物质的唯一粒子 |
1.对于反应:X+Ca(OH)2=Y+Cu(OH)2↓,下列分析中正确的是( )
| A. | 该反应类型可能是化合反应 | B. | X和Y的相对分子质量之差为18 | ||
| C. | X中一定有Cu元素和H元素 | D. | Y中一定有Ca元素 |
8.下列说法正确的是( )
①所有原子的原子核都是由质子和中子构成
②相同原子可以构成不同的分子
③分子、原子都是不带电的粒子,所以不带电的粒子一定是分子或原子
④原子、分子、离子都是构成物质的粒子
⑤某粒子示意图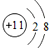 ,表示的是一种金属阳离子.
,表示的是一种金属阳离子.
①所有原子的原子核都是由质子和中子构成
②相同原子可以构成不同的分子
③分子、原子都是不带电的粒子,所以不带电的粒子一定是分子或原子
④原子、分子、离子都是构成物质的粒子
⑤某粒子示意图
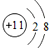 ,表示的是一种金属阳离子.
,表示的是一种金属阳离子.| A. | ①②③ | B. | ③④⑤ | C. | ①③④ | D. | ②④⑤ |
5.观察和实验是学习科学的重要方式,下列实验中观察到的颜色正确的是( )
| A. | 铁锈放入稀盐酸中溶液变黄色 | |
| B. | 硫酸铜溶液中滴加氢氧化钠溶液出现红褐色絮状沉淀 | |
| C. | 硫在氧气中燃烧发出微弱的淡蓝色火焰 | |
| D. | 酚酞试液滴入硫酸溶液中变红色 |