题目内容
某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再 向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g.
向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g.
(1)反应中生成 g二氧化碳,此反应的基本反应类型为 ;
(2)通过计算说明实际钙含量是否与标注相符;
(3)试计算所用稀盐酸的溶质质量分数.

| 根据化学反应方程式的计算;有关溶质质量分数的简单计算. | |
| 专题: | 溶质质量分数与化学方程式相结合的计算. |
| 分析: | (1)根据质量守恒定律进行分析,烧杯中的物质减少的质量就是生成的二氧化碳的质量; (2)由二氧化碳的质量,根据反应的方程式.求出碳酸钙的质量进而计算出每片中钙的质量,即可判断钙片中钙的含量标注是否属实. (3)由二氧化碳的质量,根据反应的方程式.求出消耗氯化氢的质量即可解答 |
| 解答: | (1)因为碳酸钙和稀盐酸反应放出二氧化碳,根据质量守恒定律可知,烧杯中的物质减少的质量就是生成的二氧化碳的质量,所以生成二氧化碳的质量为:2g×10+50g﹣64.5g=5.5g;有反应的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑可知该反应为复分解反应; (2)设10片片剂中碳酸钙的质量为x,消耗盐酸中的氯化氢质量为y, CaCO3+2HCl═CaCl2+H2O+CO2↑ 100 73 x y 5.5g
x=12.5g,y=9.125g 每片中钙含量是12.5g× (3)所用稀盐酸的溶质质量分数: 答案:(1)5.5,复分解反应; (2)实际钙含量与标注不相符; (3)所用稀盐酸的溶质质量分数18.25%. |
| 点评: | 本题主要考查了人体中元素的作用、质量分数的计算,利用质量守恒定律求出反应放出二氧化碳的质量,是进行后面计算的基础,体现出运用知识分析问题的能力. |

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案下列说法中正确的是( )
|
| A. | 物质溶于水放热或吸热取决于扩散与水合过程的相对强弱 |
|
| B. | 生产普通玻璃的原料是石英砂、烧碱、石灰石 |
|
| C. | 凡是均一、稳定的液体都是溶液,溶液中只能有一种溶质 |
|
| D. | 空气按体积比计算氧气氧气最多,氮气次之 |
下列化学实验中能达到预期实验结果的是( )
|
| A. | 借助托盘天平和其他手段测定铜锌合金中锌的质量分数为36.25% |
|
| B. | 用pH试纸测定某未知溶液的pH为5.5 |
|
| C. | 20℃时,配制2%的氢氧化钙溶液 |
|
| D. | 将100g 10%的稀盐酸加热蒸发掉50g水,使得稀盐酸溶质质量分数变成20% |
下列物质在空气中燃烧能产生大量白烟的是( )
|
| A. | 硫 | B. | 碳 | C. | 铁 | D. | 磷 |
 44
44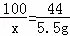 ,
,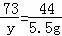
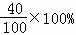 ÷10片=0.5g<0.6g,实际钙含量与标注不相符;
÷10片=0.5g<0.6g,实际钙含量与标注不相符;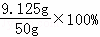 =18.25%;
=18.25%; 研究变得有规律可循 ④化学不但研究原子、分子的性质,而且要深入研究电子、质子、中子的性质
研究变得有规律可循 ④化学不但研究原子、分子的性质,而且要深入研究电子、质子、中子的性质