题目内容
14.绿矾又名七水硫酸亚铁(FeSO4•7H2O),其用途广泛,可用于制铁盐、氧化铁颜料、净水剂、防腐剂、消毒剂等.绿矾(FeSO4•7H2O)的一种综合利用工艺如下: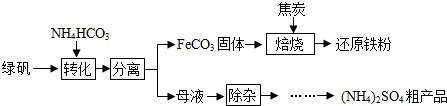
(1)细铁丝在氧气中可以燃烧,请写出铁在氧气中燃烧的化学方程式3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(2)绿矾与NH4HCO3在溶液中反应,有CO2生成,反应的化学方程式为FeSO4•7H2O+2NH4HCO3=FeCO3+(NH4)2SO4+CO2↑+8H2O.
(3)隔绝空气进行“焙烧”,铁元素的转化途径是FeCO3$\stackrel{分解}{→}$FeO$\stackrel{还原}{→}$Fe,实际作还原剂的是CO.写出“焙烧”过程中各步反应的化学方程式:
A.FeCO3$\frac{\underline{\;\;△\;\;}}{\;}$FeO+CO2↑;
B.CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
C.FeO+CO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2.
(4)母液“除杂”后,欲得到(NH4)2SO4粗产品,操作步骤依次为蒸发浓缩、降温结晶、过滤、洗涤、干燥.
分析 根据反应原理找出反应物、生成物、反应条件,然后依据质量守恒定律书写化学方程式.
解答 解:(1)细铁丝在氧气中可以燃烧生成四氧化三铁,化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(2)七水硫酸亚铁和碳酸氢铵反应生成碳酸铁、硫酸铵、水和二氧化碳,化学方程式为:FeSO4•7H2O+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+8H2O;
(3)二氧化碳和木炭在高温的条件下生成一氧化碳,化学方程式为:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
一氧化碳和氧化亚铁在加热的条件下生成铁和二氧化碳,化学方程式为:FeO+CO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2;
故答案为:
(1)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
(2)FeSO4•7H2O+2NH4HCO3=FeCO3↓+(NH4)2SO4+CO2↑+8H2O;
(3)CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;FeO+CO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2;
(4)降温结晶(或冷却热的饱和溶液).
点评 本题主要是写化学方程式,根据题意和书写化学方程式的方法书写.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
2.分类是学习化学的一种重要方法.以下分类正确的是( )
| A. | 常见的酸溶液:H2O、HCl、H2SO4 | B. | 常见的黑色固体:CuO、MnO2、Fe3O4 | ||
| C. | 常见的有还原性的物质:C、CO、O2 | D. | 常见的氧化物:MgO KMnO4 H2O |
9.甲乙丙丁四种物质混合后,在一定的条件下充分反应,测得反应前后各物质的质量分数如下表所示.说法正确的是( )
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量分数/% | 70 | 15 | 6.25 | 8.75 |
| 反应后质量分数/% | 35 | 7.5 | 48.75 | 8.75 |
| A. | 丁一定是这个反应的催化剂 | |
| B. | 参加反应的甲和乙的质量之和一定等于生成的丙的质量 | |
| C. | 甲一定是化合物,乙一定是单质 | |
| D. | 该反应可能是分解反应 |
19.下列化学用语书写正确的是( )
| A. | 2个氮分子:2N | B. | 碳酸根离子:CO3 | ||
| C. | 双氧水的化学式:H2O | D. | 磷的元素符号:P |
6.化学反应在生成新物质的同时,还伴随着能量的变化,下列反应发生时吸收热量的是( )
| A. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | B. | Mg+2HCl═MgCl2+H2↑ | ||
| C. | CaO+H2O═Ca(OH)2 | D. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO |
 配制并稀释一定质量分数的Na2SO4溶液.
配制并稀释一定质量分数的Na2SO4溶液.